
题目列表(包括答案和解析)
21.(10分)甲、乙、丙、丁、戊分别是Na2SO4、Ba(NO3)2、HNO3、BaCl2、NaOH五种溶液中的一种,现利用X溶液鉴别它们,试根据下图关系回答问题:

写出下列物质的化学式:
甲 乙 丙
丁 X
20.(12分)A-J是中学化学中常见的几种物质,它们之间的转化关系如下图所示。已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,且E可由C、F化合生成,J可作禽流感、SARS等病毒的杀菌消毒剂。

(1)写出E、B的电子式:B_______________。E 。
(2)写出反应⑦的离子方程式:_________________________________。
(3)向AlCl3溶液中加入少量固体B,写出反应的化学方程式:_________________________________。
(4)以Pt为电极电解滴加有少量酚酞的H饱和溶液,则阳极的电极反应式为:__________________。________极(填“阴”或“阳”)附近溶液由无色变为红色。
19.(8分)工业上从4J29合金(铁钴镍合金)废料中提取钴和镍,一般先用硫酸溶解合金使成为Fe2+、Co2+、Ni2+,再把Fe2+氧化为Fe3+,从而使Fe3+转化为某种沉淀析出,达到与Ni2+、Co2+分离的目的.生产上要使Fe2+氧化为Fe3+,而不使Co2+、Ni2+氧化的试剂是NaClO或NaClO3(均含少量H2SO4)溶液,反应的部分化学方程式如下(A为还原剂,方程式未配平):
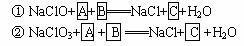
请完成以上化学方程式,并回答实际生产上采用NaClO3来氧化Fe2+比较合算的理由 ③ 。
④NaClO3还能与盐酸反应生成ClO2和Cl2,写出反应的离子方程式: 。
18.(10分)过碳酸钠(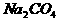 )跟稀硫酸反应的化学方程式如下:
)跟稀硫酸反应的化学方程式如下:
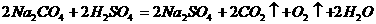
今有下图中装置可供选择,请回答:
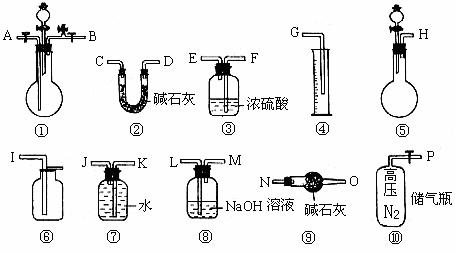
(1)某过碳酸钠中含有少量碳酸钠杂质,欲测定该样品中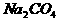 的质量分数w(
的质量分数w(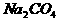 ):①应选用的仪器的连接顺序应当是(写字母)H-___________;②若样品质量为
):①应选用的仪器的连接顺序应当是(写字母)H-___________;②若样品质量为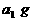 ,测得气体体积为b L(标准状况),则
,测得气体体积为b L(标准状况),则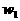 (
(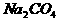 )应表示为_____________________。
)应表示为_____________________。
(2)若过碳酸钠中含有少量过氧化钠杂质,欲测定该样品中w(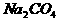 ):Ⅰ、应选用仪器的代号依次是___-__-__-②-⑨;Ⅱ、高压氮气的作用是________________;Ⅲ、若相关装置反应前后的质量分别为m1 g和m2 g,样品质量为
):Ⅰ、应选用仪器的代号依次是___-__-__-②-⑨;Ⅱ、高压氮气的作用是________________;Ⅲ、若相关装置反应前后的质量分别为m1 g和m2 g,样品质量为 ,则
,则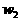 (
(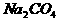 )应表示为_______________。
)应表示为_______________。
17、(11分)实验室配制480mL0.1mol/LNa2CO3溶液,回答下列问题:
(1)应用托盘天平称取无水碳酸钠粉末____ ___g。
(2)若在称量样品时,药品放在天平右盘上,砝码放在天平左盘上,天平平衡时,则实际称量的碳酸钠粉末是__ ____g(1g以下用游码)。
(3)配制Na2CO3溶液时需用的主要仪器有_______、 、 、 ___、_ _。
(4)使用容量瓶配制溶液时,下列情况会使所配溶液浓度偏低的是_________________。
①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了
②无水碳酸钠粉末已部分吸水变成晶体
③溶液转移到容量瓶后,烧杯及 玻璃棒未用蒸馏水洗涤
④转移溶液前容量瓶内有少量蒸馏水
⑤定容时,俯视容量瓶的刻度线
⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
16. 某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等),下列分析推理不正确的是:( )
|
|
50ml盐酸 |
50ml盐酸 |
50ml盐酸 |
|
m(混合物) |
9.2g |
15.7g |
27.6g |
 (标况) (标况) |
2.24L |
3.36L |
3.36L |
A.盐酸的物质的量浓度为3.0mol·L-1
B.根据表中数据不能计算出混合物中NaHCO3的质量分数
C.加入混合物9.2g时盐酸过量
D.15.7g混合物恰好与盐酸完全反应
第II卷(共86分)
15.高铁酸钾 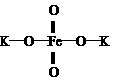 (K2FeO4)是一种新型、高效、多功能水处理剂,是比
(K2FeO4)是一种新型、高效、多功能水处理剂,是比
Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染的绿色水处理剂。工业是先制得高铁酸钠,然后在低温下,在高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾(K2FeO4)。
湿法制备的主要方程式为:2Fe(OH)3+2ClO +4OH
+4OH =
= +2Cl
+2Cl +5H2O
+5H2O
干法制备的主要方程式为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
下列有关说法不正确的是: ( )
A.高铁酸钠中铁显+6价
B.湿法中每生成1mol Na2FeO4转移3mol电子
C.干法中每生成1mol Na2FeO4转移4mol电子
D.K2FeO4处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3等,生成的Fe(OH)3还能吸附水中的悬浮杂质
14.下列各组离子能大量共存,当溶液中c(H+)=10-1mol/L时,有气体产生;而当溶液中c(H+)=10-13mol/L时,又能生成沉淀。该组离子可能是: ( )
A.Na+、Cu2+、NO3-、CO32- B.Ba2+、K+、Cl-、HCO3-
C.Fe2+、 Na+、SO42-、NO3- D.Mg2+ 、NH4+、SO42-、Cl-
13.NA表示阿伏加德罗常数,下列说法中不正确的是: ( )
A.在1L 0.5 mol/L的Na2CO3溶液中,离子总数一定大于1.5 NA
B.在常温常压下,n mol HD含有的核外电子数为2n NA
C.12.5 mL 16 mol/L浓硫酸与足量铜反应,转移的电子数为0.2 NA
D.含有1 mol碳原子的金刚石中,C-C共价键数为4 NA
12、据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢或锂电池的十倍,可连续使用一个月才充一次电,其电池反应为:2CH3OH + 3O2
+ 4OH- 2CO32- +6H2O,则下列有关说法不正确的是: ( )
2CO32- +6H2O,则下列有关说法不正确的是: ( )
A. 放电时CH3OH参与正极反应 B. 充电时阴极产生CH3OH
C. 放电时化学能转变成电能 D. 充电时每生成1molCH3OH,则转移6mol电子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com