
题目列表(包括答案和解析)
6、下列事实与氢键有关的是 ( )
A.水加热到很高的温度都难以分解
B.水结成冰体积膨胀,密度变小
C.CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高
D.HF、HCl、HBr、HI的热稳定性依次减弱
5、有如下变化:
A+ne-===An-;ΔH=-a kJ·mol- B+ne-===Bn-;ΔH=-b kJ·mol-,且a>b
下列说法正确的是 ( )
A.氧化性A<B B.还原性An->Bn-
C.稳定性A>B D.稳定性An->Bn-
4、下列各组在指定环境下能大量共存的是 ( )
A.pH=1的酸性溶液中:Na+、S2-、K+、MnO4-
B.pH=7的中性溶液中:Al3+、Cl-、SO42-、HCO3-
C.pH>7的碱性溶液中:Na+、AlO2-、SO42-、K+
D.pH=7的中性溶液中:Fe2+、ClO-、Na+、Cl-
3、下列说法中正确的是 ( )
A.一种分散质,分散到另一分散剂中,若分散系中的分散质粒子带电荷,这种分散系必为胶体
B.一种无色透明的液体,让一束光线通过时,无丁达尔现象,该液体必为溶液
C.一无色透明澄清的液态分散系,当加入电解质A时,液体中产生了白色沉淀,上述分散系必为胶体,加入A使胶体发生了凝聚
D.分散系中,分散质粒子直径介于10-9―――10-7m之间,这样的分散系必为胶体
2、下列装置(如下图所示),能够构成原电池产生电流的 ( )

1、100mL0.1mol/L醋酸与50mL0.2mol/L氢氧化钠混合,在所得溶液中 ( )
A.[Na+]>[CH3COO-]>[OH-]>[H+]
B.[Na+]>[CH3COO-]>[H+]> [OH-]
C.[Na+]>[CH3COO-]>[OH-]=[H+]
D.[Na+]=[CH3COO-]>[OH-]>[H+]
21.(8分)参照下表中物质的熔点,回答有关问题:
① 钠的卤化物及碱金属的氯化物的熔点高低取决于其______________________,
|
物质 |
NaF |
NaCl |
NaBr |
NaI |
NaCl |
KCl |
RbCl |
CsCl |
|
熔点℃ |
995 |
801 |
755 |
651 |
801 |
776 |
715 |
646 |
|
物质 |
SiF4 |
SiCl4 |
SiBr4 |
SiI4 |
SiCl4 |
GeCl4 |
SnCl4 |
PbCl4 |
|
熔点℃ |
-90.2 |
-70.4 |
5.2 |
12.05 |
-70.4 |
-49.5 |
-36.2 |
-15.0 |
在这种情况下,____________越大,________________越弱,故熔点依次降低。
② 硅的卤化物及硅、锗、锡、铅的氯化物的熔点高低取决于其_______________,
___________________越大,___________________越大,故熔点依次升高。
③ 钠的卤化物的熔点比相应硅的卤化物的熔点高得多,这是由于_______________
______________________________________________________________。
20.(10分)如图所示是某些晶体的结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨结构中的某一部分。
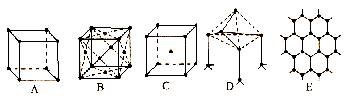
⑴ 其中代表金刚石的是(填编号字母,下同)______________,其中每个碳原子与______个碳原子最接近且距离相等。金刚石属于_________晶体。
⑵ 其中代表石墨的是_____________,其中每个正六边形占有的碳原子数平均为______个。
⑶ 其中代表NaCl的是___________。
⑷ 代表CsCl的是_____________,它属于___________晶体,每个Cs+与______个Cl-紧邻。
⑸ 代表干冰的是_________,它属于______晶体,每个CO2分子与______个CO2分子紧邻。
⑹ 上述五种物质熔点由高到低的顺序是_______________________________。
19.(6分)化工行业已合成有一种硬度比金刚石还大的晶体--氮化碳,若已知氮在该化合物中显-3价,试推断:
⑴ 其化学式可能是___________________。
⑵ 其晶体类型是______________________。
⑶ 你认为其硬度比金刚石还大的主要原因是________________________________________。
18.(10分)根据测定硫酸铜晶体中结晶水含量的实验,填写下列空白:
⑴ 有下列仪器,本实验中需要的仪器是(填写字母)________________________________,除上述仪器外,还需要的仪器是(填仪器名称): ________________________________
A、带砝码的托盘天平 B、研钵 C、试管夹 D、酒精灯 E、蒸发皿
F、玻璃棒 G、坩埚 H、干燥管 I、石棉网 J、三角架
⑵ 本实验至少需要加热_____________次,至少需要称量__________次;
⑶ 某学生实验得到以下数据:加热前容器的质量为m1,容器和晶体的总质量为m2,加热后容器和无水CuSO4的总质量为m3。请写出结晶水含量(ω)的计算公式并求出CuSO4·nH2O中n的值(用ml、m2、m3表示):
ω= ____________________,n = _____________________
⑷ 若ml = 5.4g、m2 = 7.9g、m3 = 6.8g,该生结果偏高还是偏低? _______________
从下列分析中选出该生实验产生误差的原因可能是(填写字母) ___________________
A、加热前称量时容器未完全干燥 B、最后两次加热后的质量差大于0.1g
C、加热后容器未放在干燥容器中冷却 D、加热过程中有少量晶体溅出
E、加热后的粉末中有少量黑色固体
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com