
题目列表(包括答案和解析)
13.Na3N是离子化合物,它能与水反应生成氨气。下列关于Na3N的说法中不正确的是
A.Na3N与盐酸反应时可生成两种盐
B.在Na3N与水的反应中Na3N是还原剂
C.在Na3N晶体中Na+的半径比N3-的半径大
D.Na+与N3-的电子层结构都与氖原子相同
12.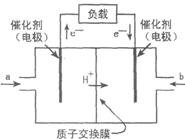 右图是2004年批量生产的笔记本电脑所用甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为: 2CH3OH+3O2=====2CO2+4H2O
右图是2004年批量生产的笔记本电脑所用甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为: 2CH3OH+3O2=====2CO2+4H2O
下列说法正确的是
A.右电极为电池的正极,b处通人的物质是空气
B.左电极为电池的负极,a处通入的物质是空气
C.负极反应式为:CH3OH+H2O-6e-=====CO2+6H+
D.正极反应式为:O2+4e-====2O2-
11.下列离子方程式中不正确的是
A.碳酸氢钠溶液与少量石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
B.用Pt电极电解MgCl2溶液2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
C.碳酸氢钠溶液与硫酸氢钠溶液反应HCO3-+H+=CO2↑+H2O
D.氯化铵与氢氧化钠两种浓溶液混合加热:NH4++OH- H2O+NH3↑
H2O+NH3↑
10.由于碘是卤素中原子半径较大的元素,可能呈现金属性。下列事实最能够说明这个结论的是
A.已经制得IBr、ICl等卤素互化物 B.已经制得I2O5等碘的氧化物
C.已经制得I(NO3)3、I(ClO4)3﹒2H2O等含I3+离子化合物
D.碘(I2)易溶于KI等碘化物溶液,形成I3-离子
9.设NA表示阿伏加德罗常数,下列说法中不正确的是
A.一定量的Fe与含1mol HNO3的稀硝酸恰好反应,如还原产物为NO,则被还原的氮原子数小于NA
B.1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒
C.常温常压下,NA个臭氧分子的体积大于22.4L
D.1.8g水中含有的电子总数为NA
8.水的状态除了气、液和固态外,还有玻璃态。它是由液态水急速冷却到165K时形成的,玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述正确的是
A.水由液态变为玻璃态,体积缩小 B.水由液态变为玻璃态,体积膨胀
C.玻璃态是水的一种特殊状态 D.玻璃态水是分子晶体
7.下列各离子组中,能在水溶液中大量共存,当滴加稀硫酸后则不能大量共存的是
A.Na+、Mg2+、Cl-、I- B.Fe2+、Ba2+、S2-、Cl-
C.Na+、Al3+、Cl-、HCO3- D.K+、Fe2+、Cl-、NO3-
6.已知25℃、101kPa下,石墨、金刚石燃烧的热化学方程式分别为:
C(石墨)+O2(g)=CO2(g);ΔH= -393.51 kJ.mol-1
C(金刚石)+O2(g)=CO2(g);ΔH= -395.41 kJ.mol-1
据此推理所得到的下列结论正确的是
A.金刚石的燃烧热比石墨的燃烧热小
B.石墨晶体中碳碳键的强度小于金刚石中的碳碳键
C.石墨的能量比金刚石的能量高
D.由石墨制备金刚石一定是吸热反应
5.钛被誉为“太空金属”,其原因是它的强度大、密度小、抗腐蚀性能好。室温下,它不与水、稀硫酸、稀硝酸反应,但易溶于氢氟酸,推断其原因是
A.氢氟酸的酸性比其它酸强 B.氢氟酸的氧化性比其它酸强
C.氢氟酸的还原性比其它酸强 D.氟离子易与钛离子形成可溶性难电离物质
4.最近有人用一种称为“超酸”的化合物H(CB11H6Cl6)和C60反应,使C60获得一个质子,得到一种新型离子化合物[HC60]+[CB11H6Cl6]-。这个反应看起来很陌生,但反应类型上却可以跟中学课本中的一个化学反应相比拟,该化学反应是
A.CO2+H2O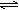 H2CO3
B.NH3+HCl=NH4Cl
H2CO3
B.NH3+HCl=NH4Cl
C.Zn+H2SO4=ZnSO4+H2↑ D.C6H5OH+NaOH=C6H5ONa+H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com