
题目列表(包括答案和解析)
11.用NA表示阿伏加德罗常数,下列说法正确的是
A.32g氧气与足量钠完全燃烧转移的电子数为2NA
B.1 mol甲基(-CH3)所含电子数10 NA
C.在标准状况下,2.24L一氧化氮与氮气混合气所含分子数为0.1NA
D.2L 1mol/L 的盐酸溶液中,所含氯化氢分子个数是2NA
10.下列比较正确的是
A.熔沸点高低:CH4 <SiH4 <GeH4<SnH4
B.离子半径大小:Cl-<Mg2+< O2-<F-
C.分散质微粒直径大小:Fe(OH)3胶体>CaCO3沉淀>NaCl溶液
D.酸性强弱:H2SO4> H3PO4> H2SiO3
9.不具有放射性的同位素称之为稳定同位素,稳定同位素分析法在近20年来植物生理学、生态学和环境科学研究中获得广泛应用。如在陆地生态系统研究中,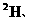
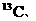
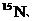
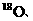
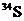 等常用作环境分析指示物。下列说法正确的是
等常用作环境分析指示物。下列说法正确的是
A.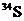 原子核内中子数为16
原子核内中子数为16
B.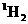
 在相同条件下比
在相同条件下比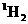
 更易蒸发
更易蒸发
C.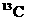 和
和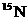 原子核内的质子数相差2
原子核内的质子数相差2
D. +的酸性比
+的酸性比 +的酸性更强
+的酸性更强
8.某盐酸的浓度为12.0 mol·L-1,其密度为1.19 g·cm-3。现有该浓度的盐酸100 L,则用于吸收HCl形成该盐酸的水的体积约是
A.75.2 L B.85.5 L C.90.8 L D.100 L
7. c(NH4+)相同的下列溶液:① 硫酸亚铁铵[(NH4)2 Fe (SO4)2 ] ②硫酸铵 ③硫酸氢铵 ④碳酸氢铵,其物质的量浓度由大到小的顺序是
A.①②③④ B.②④③① C.④③①② D.④③②①
6.已知H2(g)+Cl2(g)=2HCl(g);△H=-184.6KJ·mol-1,则反应
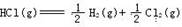 的△H为
的△H为
A.+184.6KJ·mol-1 B.-92.3KJ·mol-1
C.+92.3 KJ D.+92.3KJ·mol-1
5.对室温下pH相同、体积相同的氨水和氢氧化钠溶液分别采取下列措施,有关叙述正确的是
A.加入适量的氯化铵晶体后,两溶液的pH均碱小
B.温度下降10oC,两溶液的pH均不变
C.分别加水稀释10倍,两溶液的pH仍相等
D.用盐酸中和,消耗的盐酸体积相同
4.下列分子中,所有原子都满足最外层为8电子结构的是
A.BF3 B.PCl5 C.HCl D.CF2Cl2
3.对于下列事实的解释错误的是
①蔗糖中加入浓H2SO4后出现发黑现象,说明浓硫酸具有脱水性
②浓硝酸的颜色变黄,说明浓硝酸见光易分解
③SO2气体通入溴水使溴水褪色,说明SO2具有漂白性
④乙醛能发生银镜反应,说明乙醛具有氧化性
A.①②③④ B.③④ C.只有③ D.只有④
2.下列物质混合后产生CO2速率最快的是
A.100mL 2mol·L-1Na2CO3与100mL 2mol·L-1HCl
B.100mL 2mol·L-1NaHCO3与100mL 2mol·L-1HCl
C.400mL 1mol·L-1Na2CO3与100mL 2mol·L-1HCl
D.400mL 1mol·L-1NaHCO3与100mL 2mol·L-1HCl
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com