
题目列表(包括答案和解析)
20.(17分)某校学生活动小组设计如图所示装置探究工业制硫酸接触室中反应产物,并测定此条件下二氧化硫的转化率。实验时,装置D锥形瓶中溶液产生白色沉淀,装置E中溶液褪色。
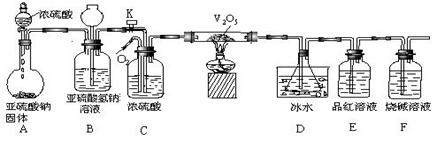
试回答下列问题:
(1)装置C有三个作用①干燥SO2和O2;②使SO2与O2充分混合;
③ 。
(2)D中锥形瓶盛放的溶液可以是(选填序号) 。
A.少量高锰酸钾溶液 B.少量小苏打溶液
C.少量氯化钡溶液 D.少量硝酸钡溶液
D锥形瓶必须浸入冰水中的原因是
(3) 反应停止后,先关闭K,继续通入O2,其目的是
。
(4)反应停止后,要通过装置D锥形瓶中产生的白色沉淀的量,测定已被氧化的二氧化硫的量时,在滤出沉淀前必须进行的一步实验操作是(简述过程)
。
(5)若从锥形瓶溶液中得到的沉淀质量为m g,要测定该条件下二氧化硫的转化率,实验时还需要测定的数据是(选填序号) ,二氧化硫的转化率是 (用含有m、a、b、c、d中的一种或几种字母的代数式表示)。
① 装置F增加的质量a g ② 装置A中亚硫酸钠减少的质量b g
③ 装置B增加的质量c g ④ 装置E增加的质量d g
(6) ①若(3)通O2时间过长,可能使检测得到的SO2的转化率
②若D装置中不用冰水,则可能使检测得到的SO2的转化率
③用酒精灯不停地加热,则可使检测到的SO2转化率 (均填偏大、偏小、不变)
19.(4分)下列有关实验说法错误的是___________
A.进行中和热测定实验时,需要测出反应前盐酸和NaOH溶液的温度及反应后溶液的最高温度
B.除去铝器皿表面的碳酸钙而不损伤铝器皿,可用冷的浓硫酸。
C.水中含有少量苯和硝基苯,可用活性碳吸附除去
D.观察钾元素焰色反应的操作是:将铂丝放在稀盐酸中洗涤,然后蘸取固体氯化钾,置于煤气灯的火焰上进行灼烧,透过蓝色钴玻璃进行观察。
E.检验某溶液中含SO42-的操作与现象是:取试样少量,滴加氯化钡溶液有白色沉淀,再加入盐酸,沉淀不消失,可确证其中含有SO42-
F.准确取用20.00mL的溴的四氯化碳溶液的方法是:取一支25mL的碱式滴定管,先用溴的四氯化碳溶液润洗,再加溶液至1.00mL处,用手挤压玻璃球,放溶液至21.00mL处。
18. 实验室中,某学生先用蒸馏水润湿精密pH试纸,(每次使用时润湿程度相同)然后用洁净干燥的玻璃棒蘸取试液进行测定试液的pH。下列说法正确的是
A.该生的测定值一定有误差产生
B.用此方法检测PH相等的盐酸和硝酸两溶液时,盐酸的pH与硝酸仍相等
C.用此方法检测c(H+)相等的盐酸和醋酸两溶液时,盐酸的pH比醋酸小
D.用此方法检测c(H+)相等的盐酸和醋酸两溶液时,醋酸的pH比盐酸小
第II卷(非选择题 共78分)
17.将PH=13的NaOH溶液平均分成两份,一份加入PH=11的KOH溶液,另一份加入与NaOH溶液等浓度的HCl,混合后溶液PH均降为12。则加入KOH溶液和HCl的体积之比为
A .11∶2 B.9∶11 C.110∶9 D.9∶1
16.某元素的离子R2+有6个电子层,最外层有2个电子。当R与过量硝酸反应时,可生成R(NO3)2,配制R(NO3)2溶液时,为得到澄清溶液常将R(NO3)2溶于硝酸并加水稀释,下列叙述正确的是
A、R为ⅡA族元素 B、R的最高价氧化物有强氧化性
C、R2+的硝酸盐水溶液呈中性 D、保存R(NO3)2溶液时,为防止氧化应加入R单质
15.将SO2通入CuSO4和NaCl的浓溶液中会析出白色沉淀,取该沉淀分析,知其中含Cl:35.7%,Cu:64.3%,SO2在上述反应中作用是
A.氧化剂 B.还原剂 C.酸 D .催化剂
14.下列离子方程式书写正确的是
A.硫酸铝溶液中滴加过量浓氨水:Al3++4OH-=AlO2-+2H2O
B.NaHCO3溶液水解:HCO3-+H2O=H2CO3+OH-
C.浓氢氧化钠溶液吸收少量SO2气体:SO2+2OH-=SO32-+H2O
D.氯气与水反应:Cl2+H2O=2H++Cl-+ClO-
13.某混合溶液中只含有两种溶质NaCl和H2SO4,且n(NaCl):n(H2SO4)=3:2。若以石墨电极电解该溶液,下列推断中不正确的是
A.阴极产物为H2 B.阳极先析出Cl2,后析出O2
C.电解液的pH不断增大,最终大于7 D.整个电解的过程实质是电解水
0.6molA 、0.3molB 和1.4molC为起始物质,达到平衡后,C的体积分数也
为W% 。平衡后若缩小容器体积,C的浓度c(C)、C的体积分数C%、混合气体平均相
对分子质量(M)和正反应速率[V(正)],随压强(P)的变化,一定符合的是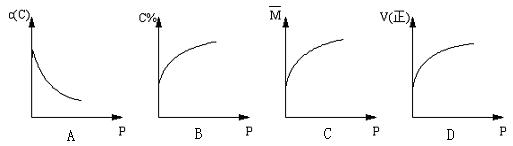
12.在一个体积为1L的密闭容器中,充入2molA和1molB,发生如下反应:
2A(g)
+ B(g) 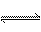 xC(g) ,平衡后,C的体积分数为W%,若维持容器容积和温度不变,
xC(g) ,平衡后,C的体积分数为W%,若维持容器容积和温度不变,
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com