
题目列表(包括答案和解析)
22.(10分)已知A为中学化学中的常见金属,X、Y为常见非金属。X、E、F、G、J常温下为气体,C为无色液体,B是一种盐,受热易分解。现用A与石墨作电极,B的浓溶液作电解质,构成原电池。有关物质之间的转化关系如下图(部分反应的条件、生成物被略去):
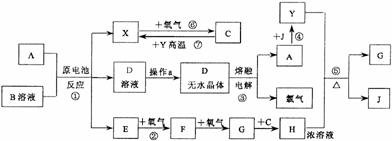
请填写下列空白:
⑴金属A为 ;操作a是将D溶液在HCl气流中蒸干,原因是
⑵反应②的化学方程式为: ;
反应⑤的化学方程式为: 。
⑶原电池反应①中,正极反应式为: 。
21.(9分)有A、B、C、D、E、F六种元素,已知:它们位于三个不同短周期,核电荷数依次增大;A与E、B与F分别同主族;A、E分别都能与D按原子个数比1﹕1或2﹕l形成化合物;B、C分别都能与D按原子个数比1﹕1或1﹕2形成化合物。
⑴写出只含有A、B、D、E四种元素的两种无水盐的化学式 、 。
⑵右图是A与D形成的一种化合物的晶体结构示意图,其中的虚线表示
,与每个“构成粒子”相邻的粒子呈
空间构型。E与D按原子个数比1﹕1形成的化合物的电子式为 。
⑶人们通常把拆开l mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下表列出了上述部分元素形成的化学键的键能:
|
化学键 |
F-D |
F-F |
B-B |
F-B |
C═D |
D═D |
|
键能/kJ·mol-1 |
460 |
176 |
347.7 |
347 |
745 |
497.3 |
①下列三种物质形成的晶体,熔点由高到低的顺序(用a、b、c表示):
a.F与B形成的化合物 b.B与D形成的稳定化合物 c.F的单质
②试估算F单质晶体的燃烧热: 。
20.(14分) I.课本中介绍了乙醇氧化的实验:把一端弯成螺旋状的铜丝放在酒精灯外焰加热,待铜丝表面变黑后立即把它插入盛有约2 mL乙醇的试管里,反复操作几次。注意闻生成物的气味,并观察铜丝表面的变化。
⑴实验室可用化学方法替代“闻生成物的气味”,写出该化学方法的化学反应方程式
。
⑵某同学在探究“闻生成物的气味”的替代方法时,偶然发现向溴水中加入乙醛溶液,溴水褪色。该同学为解释上述现象,提出两种猜想:①溴水将乙醛氧化为乙酸;②溴水与乙醛发生加成反应。请你设计一个简单的实验,探究哪一种猜想正确?
。
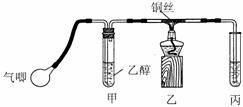 Ⅱ.某课外活动小组利用下图装置进行乙醇的催化氧化实验并制取乙醛(试管丙中用水吸收产物),图中铁架台等装置已略去。实验时,先加热玻璃管中的铜丝,约lmin后鼓入空气。请填写下列空白:
Ⅱ.某课外活动小组利用下图装置进行乙醇的催化氧化实验并制取乙醛(试管丙中用水吸收产物),图中铁架台等装置已略去。实验时,先加热玻璃管中的铜丝,约lmin后鼓入空气。请填写下列空白:
⑴乙醇发生催化氧化的化学反应方程式为
。
⑵实验时,常常将甲装置浸在70℃-80℃的水浴中,目的是 ____;由于装置设计上的缺陷,实验进行时可能会 ____________
⑶反应发生后,移去酒精灯,利用反应自身放出的热量可维持反应继续进行。进一步研究表明,鼓气速度与反应体系的温度关系曲线如图所示。

试解释鼓气速度过快,反应体系温度反而下降的原因:
;你认为该实验中“鼓气速度”这一变量可用 来计量_____________________________。
19.(8分)请按要求填空:
⑴测定硫酸铜晶体里结晶水的含量,现有托盘天平、研钵、坩埚、酒精灯(火柴)、坩埚钳、三脚架、泥三角、药匙、硫酸铜晶体样品等实验用品。进行该实验时,还缺少的实验用品是 ;整个过程至少应在天平上进行 次称量。
⑵肥皂的制取实验开始时,在蒸发皿中加入的试剂除植物油外,还有 ,其中有一种未参加反应,该物质的作用是
18.T℃时,在1L密闭容器中A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图I所示;若保持其他条件不变,温度分别为Tl和T2时,B的体积百分含量与时间的关系如图Ⅱ所示。则下列结论正确的是
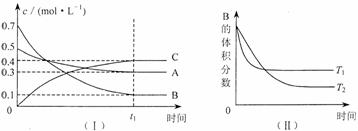
A.在达平衡后,保持其他条件不变,增大压强,平衡向正反应方向移动
B.在达平衡后,保持压强不变,通入稀有气体,平衡向正反应方向移动
C.保持其他条件不变,若反应开始时A、B、C的浓度分别为0.4mo1·L-1、0.5 mo1·L-1和0.2 mo1·L-1,则达到平衡后,C的浓度大于0.4 mo1·L-1
D.保持其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大
17.t℃时,将溶质质量分数为a%的NaOH溶液蒸发掉mg水后恢复至原温度,恰好得到质量分数为2a%的NaOH饱和溶液VmL,则下列说法中正确的是
A.t℃时NaOH的溶解度为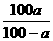 g
g
B.原溶液的质量为2mg
C.可以求算原溶液的物质的量浓度
D.保持t℃,向原溶液中加入2agNaOH可达饱和
16.已知在酸性条件下有以下反应关系:
①KBrO3能将KI氧化成I2或KIO3,本身被还原为Br2;②Br2能将I-氧化为I2;
③K1O3能将I-氧化为I2,也能将Br-氧化为Br2,本身被还原为I2。
向KI的硫酸溶液中滴加少量KBrO3溶液后,所得产物除水外还有
A.Br-、I2 B.Br2、Br-、I2 C.Br2、I2、IO3- D.Br2、IO3-
15.粗盐中含有可溶性杂质CaCl2、MgCl2和Na2SO4,若要得到纯净的NaCl固体,有如下实验操作:①加入过量Ba(OH)2溶液、②加入过量NaOH溶液、③加入过量BaCl2溶液、④加入过量Na2CO3溶液、⑤加入过量盐酸、⑥过滤、⑦蒸发结晶。正确的实验操作顺序是
A.③②④⑥⑤⑦ B.③④②⑤⑦ C.②③④⑤⑥⑦ D.①④⑥⑤⑦
14.常温时,将V1mLc1mo1·L-1的氨水滴加到V2mLc2 mol·L-l的盐酸中,下列叙述正确的是
A.若c1V1=c2V2,则所得混合液的pH=7
B.若混合液的pH=7,则混合液中c(NH4+)=c(Cl-)
C.若c1V1>c2V2,则混合液中可能呈酸性、中性或碱性
D.若V1=V2,且混合液的pH<7,则一定有c1<c2
13.用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.0.4g重水的分子中所含中子数一定为0.2NA
B.4.48LN2与CO的混合物所含分子数一定为0.2NA
C.6.4gS6与S8的混合物中所含S原子数一定为0.2NA
D.标准状况下,2.24L氧单质所含原子数一定为0.2NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com