
题目列表(包括答案和解析)
16.2005年诺贝尔化学奖授予在“烯烃复分解反应”研究方面作出贡献的三位科学家。“烯烃复分解反应”是指在金属钼、钌等催化剂的作用下,碳碳双键断裂并重新组合的过程。如两分子烯烃RCH=CHR′用上述催化剂作用会生成两种新的烯烃RCH=CHR和R′CH=CHR′。则由CH =CHCH
=CHCH CH
CH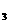 和CH
和CH =
=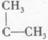 发生“烯烃复分解反应”,生成新烯烃种类为
发生“烯烃复分解反应”,生成新烯烃种类为
A.2种 B.3种 C.4种 D.5种
15.如图所示装置,两玻璃管中盛满滴有酚酞溶液的氯化钠饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。接通S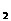 后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S
后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S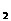 ,接通S
,接通S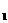 ,电流表的指
,电流表的指 针发生偏转。此时有关该装置的说法错误的是
针发生偏转。此时有关该装置的说法错误的是
A.该装置为一原电池
B.C(Ⅰ)为原电池的负极
C.C(Ⅱ)的电极反应式是:Cl +2e
+2e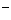 =2Cl
=2Cl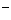
D.C(Ⅰ)附近溶液会进一步变红
14.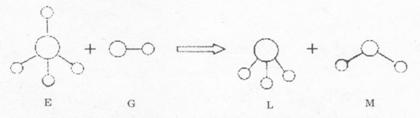 已知结构为正四面体型的离子E和直线型离子G反应,生成三角锥分子L和V形分子M(组成E、G、L、M微粒的元素原子序数均小于10),反应过程用下图表示,则下列判断错误的是
已知结构为正四面体型的离子E和直线型离子G反应,生成三角锥分子L和V形分子M(组成E、G、L、M微粒的元素原子序数均小于10),反应过程用下图表示,则下列判断错误的是
A.E、G、L、M都是10e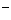 微粒
B.L、M都是极性分子
微粒
B.L、M都是极性分子
C.L能使紫色石蕊试液变蓝色 D.E离子中,质子数一定大于中子数
13.影响分子晶体熔沸点时的因素主要是分子间的各种作用力。硝基苯酚的分子内和分子之间都存在氢键,邻硝基苯酚以分子内氢键为主,对硝基苯酚以分子间氢键为主,则邻硝基苯酚和对硝基苯酚的沸点比较正确的是
A.邻硝基苯酚高于对硝基苯酚 B. 邻硝基苯酚低于对硝基苯酚
C. 邻硝基苯酚等于对硝基苯酚 D. 无法比较
12.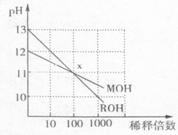 MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如右图所示。下列叙述中不正确的是
MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如右图所示。下列叙述中不正确的是
A.ROH是一种强碱
B.在x点,MOH未完全电离
C.在x点,c(M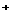 )=c(R
)=c(R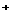 )
)
D.稀释前,c(ROH)=10c(MOH)
11.下列反应的离子方程式书写正确的是
A.烧碱溶液和过量Ca(HCO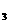 )
) 溶液反应Ca
溶液反应Ca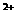 +2OH
+2OH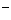 +2HCO
+2HCO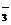 =CaCO
=CaCO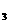 ↓+CO
↓+CO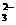 +2H
+2H O
O
B.偏铝酸钠水解:AlO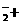 2H
2H O
O Al(OH)
Al(OH)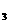 +H
+H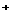
C.硫酸铝溶液中加入过量氨水Al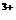 +3NH
+3NH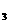 ·H
·H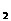 O=Al(OH)
O=Al(OH)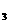 ↓+3NH
↓+3NH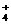
D.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液Fe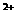 +2H
+2H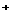 +2H
+2H O=Fe
O=Fe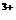 +2H
+2H O
O
10.设N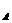 为阿伏加德罗常数,下列说法正确的是
为阿伏加德罗常数,下列说法正确的是
A.0.5 LpH=1的H SO
SO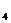 溶液中含0.1 N
溶液中含0.1 N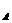 个H
个H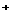
B.1 molNa O
O 与足量水充分反应,转移的电子数为2N
与足量水充分反应,转移的电子数为2N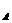
C.以铝、稀H SO
SO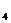 、NaOH溶液制备Al(OH)
、NaOH溶液制备Al(OH)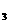 ,若消耗amolH
,若消耗amolH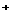 ,则至少需消耗OH
,则至少需消耗OH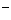 的数目为aN
的数目为aN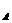
D.在20℃,1.01×10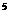 Pa时,2.8gC
Pa时,2.8gC H
H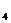 和CO的混合气体,含气体分子数小于0.1N
和CO的混合气体,含气体分子数小于0.1N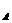
9.在容积为2 L的密闭容器中,发生如下可逆反应:mA(g)+nB(g) pC(g)+qD(g),经过5 min达到平衡,此时A减少a mol·L
pC(g)+qD(g),经过5 min达到平衡,此时A减少a mol·L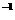 ,B的平均反应速率为
,B的平均反应速率为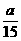 ·mol·L
·mol·L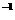 ,C增加
,C增加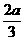 mol·L
mol·L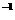 ,这时若增加系统压强,发现A与C的百分含量不变,则m∶n∶p∶q为
,这时若增加系统压强,发现A与C的百分含量不变,则m∶n∶p∶q为
A.3∶1∶2∶2 B.1∶3∶2∶2 C.1∶3∶2∶1 D. 1∶1∶1∶1
8.最新研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羰基硫(COS)。已知羰基硫分子中所有原子均满足八电子结构,下列有关说法正确的是
A.羰基硫的电子式为 B.羰基硫属于非极性分子
B.羰基硫属于非极性分子
C.羰基硫中三个原子处于同一直线上
D.羰基硫沸点比CO 低
低
7.已知乙烯和乙炔燃烧的热化学方程式分别为:
2C H
H (g)+5O
(g)+5O (g)=4CO
(g)=4CO (g)+2H
(g)+2H O(1);ΔH=-2600 kJ·mol
O(1);ΔH=-2600 kJ·mol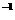
C H
H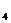 (g)+3O
(g)+3O (g)=2CO
(g)=2CO (g)+2H
(g)+2H O(1); ΔH=-1411
kJ·mol
O(1); ΔH=-1411
kJ·mol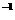
又知氧炔焰的温度比乙烯燃烧时火焰的温度高。据此,下列说法错误的是
A.物质的燃烧热越大,火焰温度越高
B.烃完全燃烧时,火焰温度的高低不仅仅取决于其燃烧热的高低
C.相同条件下等体积乙烯和乙炔完全燃烧时,乙炔放热较少
D.1mol乙烯完全燃烧生成气态产物时,放出的热量小于1411kJ
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com