
题目列表(包括答案和解析)
7、物质的氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度有关,下列各组物质由于浓度不同而能发生不同氧化还原反应的是( )
A、Zn和H2SO4 B、Cu和FeCl3溶液 C、CO2和NaOH溶液 D、Fe和HCl溶液
6、在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的是( )
A、滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、SCN-
B、PH为1的溶液:Cu2+、Na+、Mg2+、NO3-
C、水电离出来的C(H+)=10-13mol/L:K+、HCO3-、Br-、Ba2+
D、所含溶质为Na2SO4的溶液:K+、CO32-、NO3-、Al3+
5、用惰性电极电解下列溶液一段时间后,阴极质量增加、溶液的PH明显下降的是( )
A、H2SO4 B、AgNO3 C、BaCl2 D、CuCl2
4、下列关于胶体的叙述,不正确的是( )
A、用渗析的方法净化胶体时,使用的半透膜只能让较小的分子、离子通过
B、一束光线通过气体时,胶体会形成一条“光亮”的通路
C、布朗运动是胶体粒子特有的运动方式,可以据此把胶体和溶液、悬浊液区别开来
D、胶体粒子具有较大的表面积,有的能吸附阳离子或阴离子而使胶体粒子带电荷,故在电场作用下会产生电泳现象
3、铁棒和石墨用导线连接后,浸入0.01mol/L的食盐溶液中,可能出现的情况是( )
A、铁棒附近产生OH- B、铁棒被腐蚀 C、石墨上放出O2 D、石墨棒上放出Cl2
2、以下有关接触法制硫酸的论述,错误的是( )
A、为提高反应速率和原料利用率,硫铁矿要在“沸腾炉”状态下燃烧
B、为防止催化剂中毒,气体在进接触室前要先净化
C、接触室中热交换器的主要作用是预热未反应的气体和冷却反应后的气体
D、吸收塔中SO3从下而上,水从上而下,剩余气体从上部出来放空
1、固体融化时,必须破坏非极性共价键的是( )
A、冰 B、晶体硅 C、溴 D、二氧化硅
25·(8分)为确定复盐CuS04。z(NH4)2804·yH20的化学式,化学实验探究小组的同学进行了下列实验:
(1)准确称取试样两份,质量各10.0 g。
(2)将其中一份溶于水,向所得溶液中加入过量的BaCl2溶液,生成的沉淀经过滤、洗涤、干燥后称得质量为11.65 g。
(3)将另一份试样加到过量的NaOH浓溶液中,加热生成的气体用100 mL 0.5m01.L-1的硫酸吸收,多余的硫酸用2 molL-1NaOH溶液滴定,用去NaOH溶液25.00mL达滴定终点。试计算上述复盐化学式中 x和y的值。
26·(10分)有两种不同质量分数的氧化铜与炭粉的混合物,甲、乙两位同学各取一种样品,加强热充分反应,测定各样品中氧化铜的量。
试回答下列问题:
(1)反应中可能发生反应的化学方程式为:---------------------------------------
-----------------------’---------------------------一'
(2)甲取样品口g,隔绝空气强热,生成的气体不能使澄清石灰水变浑浊。将反应后的固体
与足量的稀硝酸微热,充分反应后,有b g固体剩余,该剩余固体的化学式为 。
样品中氧化铜的质量为--g(以含a、b的代数式表示)。
(3)乙取另一样品,经隔绝空气强热后,测得剩余固体的质量比原样品的质量减少了c g。
若该固体为金属铜,试计算所取样品中氧化铜的物质的量n(Cu)的取值范围。
淮安市2005-2006学年度高三年级第一次调查测试
23·(8分)下图中的每一种物质都是中学化学常见的物质。其中A占海洋中盐类物质的80%
以上,B、C、D、E、F等都是工业生产中重要的化工产品和原料,且E是一种常见的金属(图
中部分反应物或生成物和反应条件没有列出)。
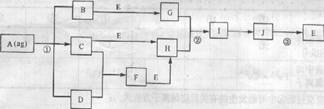
请按要求回答:
(1)反应①的化学方程式为(请注明反应进行的条件)
(2)反应②的离子方程式为

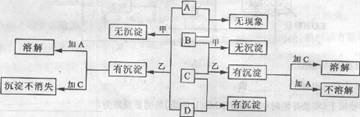
请按要求回答:
(1)甲做B、C混合实验时的具体实验现象是
有关反应的离子方程式分别是
(2)乙做A、D混合实验时操作是 。
实验中生成沉淀和沉淀加A溶解的离子方程式分别是 。
22.(8分)下图所示实验中,A、B中的电极为多孔铂电极,c、d为夹在经Na2S04溶液浸湿的滤纸条上的铂夹,a、b为电源的两极。将A、B中充满KOH溶液后倒立于盛有KOH溶液的
水槽中,断开开关K1,闭合K2、K3,通以直流电。
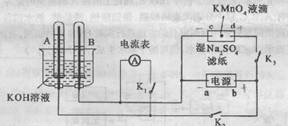
请回答下列问题:
(1)a为直流电源 极。
(2)滤纸上(实验开始时中央滴有KMn04液滴)的明显现象为
(3)写出电极反应式:A极: ;
C极: 。
(4)若经电解一段时间后,A、B中均有气体包围电极,此时切断K2、K3,闭合K1,则电流表的指针是否发生偏转,说明你的理由
-------------------------------------------一。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com