
题目列表(包括答案和解析)
3、最近俄罗斯科学家用铪和钨两种核素精确测定了地球和月球的年龄,得出月球至少比地球早700万年形成,它们是根据182 72Hf(铪-182)和182 74W(钨-182)两种核素的含量比例得出的。下列有关铪-182和钨-182的关系说法正确的是
A、互为同位素 B、都属于镧系元素
C、中子数相等 D、原子质量几乎相同
2、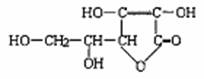 2006年3月2日英国《泰晤士报》报道说,英国食品标准局在对英国与法国贩售的芬达汽水、美年达橙汁等230种软饮料检测,发现含有高量的致癌化学物质--苯,报道指出汽水中如果同时含有苯甲酸钠(防腐剂,C6H5COONa)与维生素C(抗氧化剂,结构式如图)可能会相互作用生成苯、苯与血癌(白血病)的形成也有密不可分的关系。下列说法一定不正确的是
2006年3月2日英国《泰晤士报》报道说,英国食品标准局在对英国与法国贩售的芬达汽水、美年达橙汁等230种软饮料检测,发现含有高量的致癌化学物质--苯,报道指出汽水中如果同时含有苯甲酸钠(防腐剂,C6H5COONa)与维生素C(抗氧化剂,结构式如图)可能会相互作用生成苯、苯与血癌(白血病)的形成也有密不可分的关系。下列说法一定不正确的是
A、苯是非极性分子
B、苯在一定条件下能发生取代反应和加成反应
C、维生素C在碱性溶液中能稳定存在
D、维生素C可溶于水
1、今年是第37个“世界地球日”,宣传主题是“善待地球--珍惜资源、持续发展”。下列活动或行为不符合这一主题的是
A、发展循环经济,构建资源节约型社会及清洁生产技术
B、采用绿色化学生产工艺,建立环境友好型化工体系
C、大力开发可再生资源,推广用乙醇汽油代替传统的燃油
D、设计化学实验方案时,提倡用尽可能多的样品和试剂以提高实验效果
28.(13分)硫酸工业生产应考虑综合经济效益。
(1)若从下列四个地区选址新建一座硫酸厂,最合适的地点应在_________附近。
a.风景旅游区 b.硫酸消耗中心区 c.人口稠密区 d.黄铁矿矿区
(2)工业生产硫酸的原料气成分(体积分数)为:SO2 7%,O2 11%,N2 82%。
 压强及温度对SO2转化率的影响如下:
压强及温度对SO2转化率的影响如下:
|
|
0.1 |
0.5 |
1 |
10 |
|
400 |
99.2 |
99.6 |
99.7 |
99.9 |
|
500 |
93.5 |
96.9 |
97.8 |
99.3 |
|
600 |
73.7 |
85.8 |
89.5 |
96.4 |
工业上,二氧化硫催化氧化过程采用的是常压而不是高压,主要原因是
____________________________________________________________________。
分析上表数据可知,二氧化硫的催化氧化是放热反应,理由是____________________________________________________________________。
(3)据测算,接触法制硫酸过程中,每生产1 t 98%的硫酸需消耗3.60×105 kJ能量。
 若反应:2SO2(g)+O2(g) 2SO3(g),ΔH=-196.6 kJ /mol放出的热量完全被利
若反应:2SO2(g)+O2(g) 2SO3(g),ΔH=-196.6 kJ /mol放出的热量完全被利
用,则每生产1 t 98%的硫酸可为外界提供_____________kJ能量(不考虑其他过
程释放的能量)。
(4)依据题给数据计算:在500℃0.1MPa条件下,二氧化硫的催化氧化达到平衡时,各种气体的体积比V(SO2)∶V(SO3)∶V(O2)∶V(N2)= ∶ ∶ ∶82
27.(15分)利用下图所示装置制取氧气并进行相关的实验探究。
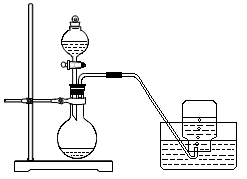
(1)将3.9 g过氧化钠放入烧瓶中,加入100 mLH2O,用排水法收集气体。 ① 过氧化钠跟水反应的化学方程式为________________________________。
② 集气瓶充满气体后,怎样从水槽中取出集气瓶?简述操作方法。 ______________________________________________________________
______________________________________________________________。
(2)已知:酚酞在c(OH-)在1.0×10-4 mol/L~2.5 mol/L时呈红色,且0.5 min内不会褪色;H2O2具有氧化性和漂白性。取上述实验得到的溶液于试管中,滴入2滴酚酞试液,溶液变红,片刻红色褪去。
① 有人认为,“红色迅速褪去”是由于溶液中c(OH-)过大造成的,试通过估算并
对比数据加以说明。
________________________________________________________________ _______________________________________________________________。 ② 还有人认为,“红色迅速褪去”是因为溶液中存在H2O2。试设计实验证明烧瓶
内的溶液中可能有H2O2存在,请简述实验操作。
__________________________________________________________________
_________________________________________________________________。
③ 补充实验,证明“红色迅速褪去”与溶液中存在H2O2有关。请简述实验操作。
__________________________________________________________________
_________________________________________________________________。
26.(16分)A、B、D、E是周期表中前20号元素,它们的原子序数依次增大。EA2与水反应产生可燃性气体和白色浆状物,向该浆状物中通入AB2气体可得另一白色不溶物。B、D同主族,D的阴离子与E的阳离子具有相同的核外电子排布。请回答:
(1)写出元素符号:A 、B 。
(2)已知AD2与AB2的结构相似,AD2的结构式为 ,该分子是 (填“极性分子”或“非极性分子”)。
(3)镁条在AB2中燃烧的化学方程式为______________________________________。
(4)将D单质放入浓HNO3中加热,生成红棕色气体和一种强酸,该反应的离子方程式为 。
(5)A可形成二元弱酸H2A2O4。0.1 molH2A2O4与100 mL 2 mol/L的KOH溶液反应后,溶液中的离子浓度由大到小的排列顺序是 。
25.(16分)有机物A(C7H11Cl3O2)在NaOH水溶液中加热,生成有机物B和C。
(1)产物B(C4H10O3)分子中含有甲基,官能团分别连在不同碳原子上,它与甘油互
为同系物。 ① B分子中的官能团名称是___________________。 ② B可能的结构简式为__________________、____________________。 ③ B不可能发生的反应有________________。 a.消去反应 b.加成反应 c.水解反应 d.氧化反应 (2)C~F有下图所示的转化关系。C、D、E、F分子中均不含甲基,其中E能跟B发
生酯化反应。
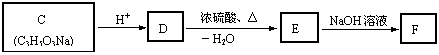
① D的结构简式为_______________________________。
② F在一定条件下可转化为PAAS(高分子化合物,常用作食品增稠剂),该反 应的化学方程式为________________________________________________。
(3)如何通过实验证明A分子中含有氯元素,简述实验操作。 ____________________________________________________________________
___________________________________________________________________。
12.将质量分数为a % 的稀硫酸蒸发掉一定量水,使其质量分数为2a %,如果用c1和c2分别表示溶液蒸发前和蒸发后的物质的量浓度,则c1与c2的关系是
A.c1=2c2 B.c2=2c1 C.c2>2c1 D.c2<2c1
11.甲、乙都是短周期元素,其中甲元素原子的最外层电子数是次外层电子数的2倍,乙元素原子K层和M层电子数之和与L层的电子数相同。下列判断不正确的是 A.乙元素的族序数比甲元素的族序数大
B.乙元素最高价含氧酸酸性比甲元素最高价含氧酸酸性强 C.乙元素的原子序数比甲元素的原子序数大
D.含乙元素的化合物数目比含甲元素的化合物数目多
10.已知:Cu+2Fe3+=2Fe2++Cu2+。将Cu片放入0.1 mol/L的FeCl3溶液中,一段时间后取出Cu片,溶液中c(Fe3+):c(Fe2+)=2:3,则n(Cu2+):n(Fe3+)为
A.3:4 B.3:5 C.4:3 D.3:2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com