
题目列表(包括答案和解析)
18.甲酸的下列性质中,可以证明它是弱电解质的是:( ) A。1mol/L甲酸溶液的c(H+)=10-2mol/L B。甲酸以任何比与水互溶;
C。10mL1mol/L甲酸恰好与10mL1mol/LNaOH溶液完全反应;
D.在相同条件下,甲酸溶液的导电性比醋酸溶液强; 19.室温下,在pH=12的某溶液中,由水电离的c(OH‑)为( ) A.1.0×10-7mol/L B.1.0×10-6mol/L C.1.0×10-2mol/L D.1.0×10-12mol/L 20.为了配制NH4+浓度与Cl-的浓度比为1:1的溶液,可在NH4Cl溶液中加入
①适量的HCl②适量的NaCl③适量的氨水④适量的NaOH,正确的是( ) A.①② B.③ C.③④ D.④ 21.在室温下,等体积的酸和碱的溶液,混合后pH一定小于7的是
A pH=3的硝酸跟pH=11的氢氧化钾溶液
B pH=3的盐酸跟pH=11的氨水
C pH=3的硫酸跟pH=11的氢氧化钾溶液
D pH=3的醋酸跟pH=11的氢氧化钡溶液
17.下列说法中可以说明N2+3H2  2NH3已达平衡的是(
)
A。在一个N≡N键断裂的同时,有3个H-H键断裂
B。在一个N≡N键断裂的同时,有2个N-H键断裂
C。在一个N≡N键断裂的同时,有6个N-H键断裂
D。在一个N≡N键断裂的同时,有6个N-H键形成
2NH3已达平衡的是(
)
A。在一个N≡N键断裂的同时,有3个H-H键断裂
B。在一个N≡N键断裂的同时,有2个N-H键断裂
C。在一个N≡N键断裂的同时,有6个N-H键断裂
D。在一个N≡N键断裂的同时,有6个N-H键形成
15.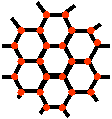 石墨晶体如图所示,每一层由无数个正六边形构成,则平均每个正六边形所占有的碳原子数为 ( )
A.6个 B.4个 C.3个 D.2个
16.对A + 3B = 2C
+2D来说,下列四种不同情况下的反应速率最快的是( )
石墨晶体如图所示,每一层由无数个正六边形构成,则平均每个正六边形所占有的碳原子数为 ( )
A.6个 B.4个 C.3个 D.2个
16.对A + 3B = 2C
+2D来说,下列四种不同情况下的反应速率最快的是( )
A.υ(A)= 0.15 mol/(L·min)
B.υ(B)= 0.6 mol/(L·min)
C.υ(C)= 0.4 mol/(L·min)
D.υ(D)= 0.45 mol/(L·min)CD
14.关于化学键的下列叙述中,不正确的是( )
A. 离子化合物可能含非极性共价键 B. 离子化合物中可能含极性共价键
C. 共价化合物可能含离子键 D. 共价化合物中可能含极性共价键
13.甲,乙是周期表中同一主族的两种元素,若甲的原子序数为x,则乙的原子序数不可能是( ) A.x+2 B x+4 C.x+8 D.x+18
12.某元素的两种同位素,它们的原子具有不同的
A.质子数 B。质量数 C。原子序数 D。电子数
11.用质量分数为98%的浓硫酸配制一定体积1.0mol/L的稀硫酸时,不需要用到的仪器( )
A.玻璃棒 B.胶头滴管 C.托盘天平 D.容量瓶
10. 金刚石的熔点为a℃,晶体硅的熔点为b℃,足球烯(分子式为C60)的熔点为c℃,三者熔点的关系是( )
A.a>b>c B.b>a>c C.c>a>b D.c>b>a
9.2008年北京奥运会“祥云”火炬用的是环保型燃料--丙烷,悉尼奥运会火炬所用燃料为65%丁烷和35%丙烷,已知丙烷的燃烧热为:2221.5KJ/mol,下列有关说法正确的是( )
A.奥运火炬燃烧主要是将化学能转变为热能和光能 B.丙烷的沸点比正丁烷高
C.丙烷、空气及铂片可组成燃料电池,在丙烷附近的铂极为电池的正极
D.丙烷燃烧的热化学方程式为C3H8(g)+5O2(g)=3CO2(g)+4H2O(g);△H= -2221.5kJ/mol
8.胶体区别于其他分散系的本质特征是( )。
A.产生布朗运动 B。产生丁达尔现象
C.胶体微粒不能穿透半透膜 D。分散质直径在10-7-10-9m之间
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com