
题目列表(包括答案和解析)
1、下列电子式或结构式错误的是
A.OH-的电子式 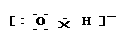 B.NH4Br的电子式
B.NH4Br的电子式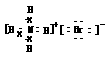
C.CCl4的电子式 D.H2S的结构式H-S-H
D.H2S的结构式H-S-H
23、(10分)取等物质的量浓度的NaOH溶液两份A和B,每份10 mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol·L-1的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如下图所示,试回答下列问题:
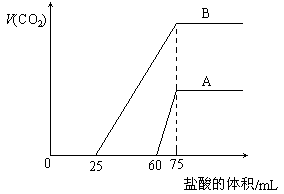
(1)原NaOH溶液的物质的量浓度为 (2分)
(2)曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质为(写化学式)
;其物质的量之比为 。(2分+3分)
(3)曲线B表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为 mL。(3分)
2006~2007学年度第一学期
22、(8分)取50.0mLNa2CO3和Na2SO4的混和溶液,加入过量的BaCl2溶液后,得到14.51g白色沉淀,用过量稀硝酸处理后沉淀量减少到4.66g ,并有气体放出。试计算:
(1)原混和溶液中Na2CO3和Na2SO4的物质的量浓度。
(2)产生的气体在标准状况下的体积。
21、(14分)下图是中学化学中常见物质之间的相互转化关系。其中,X是气体单质,Y是液体化合物,Z是常见的碱且焰色反应为黄色;W、L是固体单质,K、I中含有相同的元素;反应①是高温下进行的工业上制取H的第一步反应。请按要求填空:
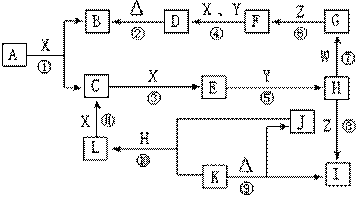
(1)G、H的化学式分别为 G 、 H ,
Y、Z的电子式分别为 Y 、Z ;
(2)写出下列反应的化学方程式:
① ;
④ ;
⑨ ;
(3)反应⑩中生成 1molL时,转移的电子数为 (NA表示阿拂加得罗常数)。
20、(10分)X、Y、Z为三个不同短周期非金属元素的单质。在一定条件下有如下反应:Y+X → A(g), Y+Z → B(g)。 请针对以下两种不同情况回答:
(1)若常温下X、Y、Z均为气体,且A和B化合生成固体C时有白烟产生,则:
① Y的化学式是 ;
② 生成固体C的化学方程式是 。
(2)若常温下Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,则:
① B的化学式是 ;
② 向苛性钠溶液中通入过量的A,所发生反应的离子方程式 ;
③ 将Y与(1)中某单质的水溶液充分反应可生成两种强酸,该反应的化学方程式是 。
19、(9分)(1)配平下列离子反应方程式
Fe(OH)3 + ClO- + OH- → FeO4 n- + Cl- + H2O
(2)已知有10.7g Fe(OH)3参加反应,共转移了0.3NA个电子,则n = ,
FeO4n-中铁元素的化合价为 。
(3)根据前面的知识,推测FeO4 n-能和下列 (填序号)物质反应。
A、KMnO4 B、SO2 C、H2S D、O2
18、(8分)目前世界上比较先进的电解制碱术是离子交换膜法。试回答下列问题:
(1)电解法制碱的主要原料是饱和食盐水,由于粗盐水中含有泥沙、Ca2+、Mg2+、Fe3+、SO42-杂质,不符合电解要求,因此必须经过精制。 除去SO42-可用钡试剂,该钡试剂可以是 。(选填a、b、c)
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(2)现有200mL食盐水,其中含有少量的NaOH,该溶液的pH等于10,用石墨电极电解,当阴极产生的气体体积为0.224L(标准状况)时停止电解。
阳极的电极反应式为 。
总反应化学方程式: 。电解后溶液的pH约为(忽略溶液的体积变化) 。
17、(15分)我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他利用NaHCO3、NaCl、NH4C1等物质溶解度的差异,以食盐、氨气、二氧化碳等为原料先制得NaHCO3,进而生产出纯碱。下面是在实验室中模拟“侯氏制碱法”制取NaHCO3的实验步骤:
第一步:连接好装置,检验气密性,在仪器内装入药品。
第二步:先让一装置发生反应,直到产生的气体不能再在C中溶解时,再通入另一装置中产生的气体,片刻后,C中出现固体。继续向C中通入两种气体,直到不再有固体产生。
第三步:过滤C中所得的混合物,得到NaHCO3固体。
第四步:向滤液中加入适量的NaCl粉末,有NH4C1晶体析出。
请回答下列问题:
(1)装置的连接顺序是:(a)接( ) ( )接( ); (b)接( )

(2)A中常选用的固体反应物为 ;D中应选用的液体为 ;B中发生反应的化学方程式为 。
(3)第二步骤中必须先让 装置先发生反应。
(4)C中用球形干燥管而不用直导管,其作用是 ,C中广口瓶内产生固体的总化学方程式为 。
(5)第四步中分离出NH4C1晶体的操作是 ;其所得的NH4C1晶体中常含有少量的NaCl和NaHCO3约占5%~8%),请设计一个简单的实验证明所得固体的成分大部分是NH4Cl。简要写出操作和现象:(3分)
。
16、(16分)已知某纯碱试样中含有NaCl杂质,为测定试样中的纯碱的质量分数,可用下图中的装置进行实验。
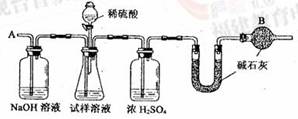
主要实验步骤如下:
①按图组装仪器,并检查装置的气密性
②将a g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U型管的质量,得到b g
④从分液漏斗滴入6 mol·L-1的硫酸,直到不再产生气体为止
⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U型管的质量,得到c g
⑦重复步骤⑤和⑥的操作,直到U型管的质量基本不变,为d g
请填空和回答问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明______ _____;
(2)装置中干燥管B的作用是_________ _______;
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果___________(填偏高、偏低或不变)
(4)步骤⑤的目的是_____________ _ __;
(5)步骤⑦的目的是__________ _____;
(6)该试样中纯碱的质量分数的计算式为_________________ ___;
(7)还可以用其他实验方法测定试样中纯碱的质量分数。请简述一种不同的实验方法。
简述实验步骤。(4分)
15、下列画有横线的物质在反应中不能完全消耗的是
A、将含少量CO2的CO气体通入盛有足量的Na2O2的密闭容器中,并不断用电火花引燃
B、将1mol Mg置于10L空气中(标况),使之在高温下反应
C、将1mol Cu置于含2mol H2SO4的98%的浓硫酸中加热
D、在强光持续照射下,向过量的Ca(ClO)2悬浊液中通入少量CO2
第Ⅱ卷(非选择题 共90分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com