
题目列表(包括答案和解析)
2.电解通电时,电子从电源的_____极沿导线流入电解池的_____极,在阴极区氧化性强的阳离子先得电子,被_________。同时,电子又从电解池的________流出,沿导线流回电源的正极,即在阳极区还原性强的阴离子(包括活性电极)先_______电子被_______。
1.(1)原电池中较活泼的金属是_____极,较不活泼的金属(或能导电的非金属)是_______极。
(2)电解池中与外电源的正极相连的极板叫____极,与外电源的负极相连的极板叫_____极。
(3)原电池是把______能转化为________能的装置。电解池是把______能转化为________能的装置。在能量转化过程中,都发生了___ _______反应。
(12分)17.(1)、 ;(2) 、 、
(3)、 ;(4) 。
(14分)18、(1)、 ,
(2)、 ;
(3)、a ;
b ;
(4)、 ;(5)、
(10分)19、(1) ;(2)
(3) ;
(4)
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
|
|
|
|
|
|
|
|
|
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
|
|
|
|
|
|
|
|
|
19.(10分)X、Y、Z、W为按原子序数由小到大排列的四种短周期元素。已知:
① X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物;
② Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物。
请回答:
⑴ Z2Y的化学式是
⑵ Z2Y2与X2Y反应的化学方程式是 。
⑶ 如图所示装置,两玻璃管中盛满滴有酚酞的溶液的ZW饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。
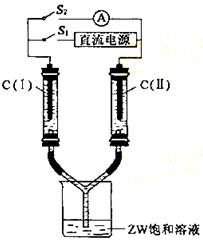
接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转。此时:C(Ⅰ)的电极名称是 (填写正极或负极);C(Ⅱ)的电极反应式是 。
(4)铜屑放入稀硫酸不发生反应,若在稀硫酸中加入X2Y2,铜屑可逐渐溶解,该反应的离子方程式
是: 。
2006学年高三年级化学同步测试题
第四单元 电解原理及其应用单元测试答题卷
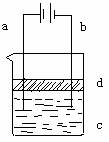
18.(14分)由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱溶液反应制得白色、纯净的Fe(OH)2沉淀。应用如图所示电解实验可制得Fe(OH)2沉淀。两电极的材料分别为铁和石墨。
⑴ a电极材料应为_________,电极反应式为_____________。
⑵ 电解液c可以是___________(选填编号)
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
⑶ d是苯,其作用为_____________________,在加入苯之前应对c溶液进 行如何处理?_____________________________。
⑷ 为了在较短时间内看到白色沉淀,可采取的措施是_____(选填编号)
A.改用稀硫酸做电解液 B.适当增加电源的电压
C.适当减小两电极间距离 D.适当降低电解液的温度
⑸ 若c用硫酸钠溶液,当电解一段时间看到白色Fe(OH)2沉淀后,再反接电源电解,除在电极上可以看到气泡外,混合物中另一明显现象为_____________________________________。
17.(12分)如图所示,若电解5min时铜电极质量增加2.16g,试回答:
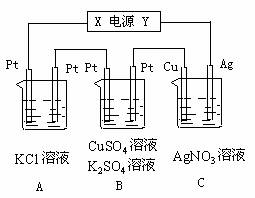
⑴ 电源电极X名称为_____________。
⑵ PH变化:A_____________,B_______________,C_______________。
 ⑶ 通过5min时,B中共收集224mL气体(标况),溶液体积为200mL,则通电前硫酸铜溶液的物质的量浓度为______________。
⑶ 通过5min时,B中共收集224mL气体(标况),溶液体积为200mL,则通电前硫酸铜溶液的物质的量浓度为______________。
⑷ 若A中KCl溶液的体积也是200mL,电解后溶液的PH = __________。
16.将含有0.400molCu(NO3)2和0.400molKCl的水溶液1L,用惰性电极电解一段时间后,在一个电极上析出0.300molCu,此时在另一电极上放出的气体在标准状况下的体积为
A.3.36L B.6.72L
C.5.60L D.大于5.60L,小于6.72L
15.碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:
Zn(s)+2MnO2(s)+H2O(l)===Zn(OH)2(s)+Mn2O3(s)
下列说法错误的是
A.电池工作时,锌失去电子
B.电池正极的电极反应式为:2MnO2(s)+H2O(l)+2e-===Mn2O3(s)+2OH-(aq)
C.电池工作时,电子由正极通过外电路流向负极
D.外电路中每通过0.2 mol电子,锌的质量理论上减小6.5 g
14.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:
3Zn + 2K2FeO4 + 8H2O == 3Zn(OH)2 + 2Fe(OH)3 + 4KOH
下列叙述不正确的是
A.放电时负极反应为:Zn - 2e- + 2OH- == Zn(OH)2
B.充电时阳极反应为:Fe(OH)3 - 3e- + 5OH- == FeO42- + 4H2O
C.放电时每转移3moL电子,正极有1 mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com