
题目列表(包括答案和解析)
22.一定量的液态化合物XY2,在一定量O2中恰好完全反应, XY2(l)+3O2(g)===XO2(g)+2YO2(g)
冷却后在标准状况下,测得生成物的体积为672 mL,密度2.56 g﹒L-1,则
(1)反应前O2的体积是 mL.
(2)化合物XY2的摩尔质量是 .
(3)在XY2分子中,X﹑Y两元素的质量比为3:16,则X﹑Y两元素分别为
和 .(名称)
21.我国化学家侯德榜(右图)改革国外的纯碱生产工艺,生产流程可简要表示如下:

⑴ 上述生产纯碱的方法称_________________,副产品的一种用途为_________________。
⑵沉淀池中发生的化学反应方程式是 __________________________________________。
⑶ 写出上述流程中X物质的分子式_______________________。
⑷ 使原料氯化钠的利用率从70%提高到90%以上,主要是设计了__________(填上述流程中的编号)的循环,从沉淀池中取出沉淀的操作是____________________。
⑸ 为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加_____________。
⑹ 向母液中通氨气,加入细小食盐颗粒,冷却析出副产品。通氨气的作用有_____________。
(a) 增大NH4+的浓度,使NH4Cl更多地析出
(b) 使NaHCO3更多地析出
(c) 使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
20.电解原理在化工中有广泛应用。下图是一个电解装置,内装溶液a;X、Y是两根石墨电极,通过导线与直流电源相连。
请回答以下问题:
若a是饱和NaCl溶液,实验开始时在两边各滴入几滴酚酞试液,则 极附近溶液变红色,装置内发生反应的化学方程式是 ;
Cl2在 极上生成,检验的方法是 。
19.要得到(Ⅰ)中结论,请从Ⅱ﹑Ⅲ中选择相应的字母填入表内,并写出有关化学反应方程式(或说明理由).
|
(Ⅰ)实验结论 |
答案 |
有关反应方程式(或简要说明理由) |
|
|
(Ⅱ) |
(Ⅲ) |
||
|
①蛋壳中含有碳酸盐 |
|
|
|
|
③粗盐中混有少量钾盐 |
|
|
|
|
④芒硝的成分含Na2SO4 |
|
|
|
(Ⅱ)实验方法:A.加盐酸;B.加热;C.进行焰色反应;D.加BaCl2溶液;E.加CaCl2溶液
(Ⅲ)实验现象:a.有气体生成;b.有不溶于水的白色沉淀生成;c.呈黄色;d.呈浅紫色(透过蓝色钴玻璃观察)
18.将0.2 mol MnO2和50 mL 12 mol﹒L-1的盐酸混合后缓缓加热,反应完全后留下的溶液中加入足量的AgNO3溶液,生成AgCl沉淀的物质的量为(不考虑盐酸的挥发) ( )
A.等于0.3 mol B.小于0.3mol C.大于0.3mol, 小于0.6mol D.以上都不正确
17.可以证明次氯酸为弱酸的实验事实是 ( )
A.次氯酸具有强氧化性 B.次氯酸不稳定,见光即分解
C.可与强碱发生中和反应 D.其盐可与弱酸发生复分解反应
16.由一种阳离子与两种酸根离子组成的盐称为混盐。混盐CaOCl2在酸性条件下可以生成Cl2。下列关于混盐CaOCl2的有关判断不正确的是 ( )
A.该混盐与硫酸反应产生1mol Cl2时转移2NA个电子 B.该混盐的摩尔质量为127
C.该混盐具有较强的氧化性 D.该混盐中氯元素的化合价为+1和-1
15.ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制取2KClO3 + H2C2O4
+ H2SO4  2ClO2↑+
K2SO4 + 2CO2↑+ 2H2O
( )
2ClO2↑+
K2SO4 + 2CO2↑+ 2H2O
( )
A.KClO3在反应中得到电子 B.ClO2是氧化产物
C.H2C2O4在反应中被氧化 D.1mol KClO3参加反应有2mol电子转移
14.下列离子方程式中,正确的是 ( )
A.醋酸与小苏打溶液反应 H++HCO3-===CO2+H2O
B.氯气溶于水 H2O+Cl2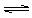 H++Cl-+HClO
H++Cl-+HClO
C.铁与三氯化铁溶液反应 Fe + Fe3+ === 2Fe2+
D.碳酸氢钠溶液与少量澄清石灰水反应 2HCO3- +Ca2+ + 2OH-===CaCO3↓+2H2O+CO32-
13.纯碱和小苏打是厨房中两种常见的用品,它们都是白色固体,下列区分这两种物质的方法正确的是 ( )
A.分别用砂锅加热两种样品,全部分解挥发没有残留物的是小苏打
B.用洁净铁丝蘸取两种样品在煤气火焰上灼烧,使火焰颜色发生明显变化的是小苏打
C.用两只小玻璃杯,分别加入少量的两种样品,再加入等量的食醋,产生气泡快的是小苏打
D.先将两样品配成溶液,分别加入澄清石灰水,无白色沉淀生成的是小苏打
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com