
题目列表(包括答案和解析)
16. KO2的晶体结构与NaCl相似,可以看作是Na+的位置用K+代替,Cl -的位置用O2
- 代替,下列对KO2晶体结构的描述正确的是
KO2的晶体结构与NaCl相似,可以看作是Na+的位置用K+代替,Cl -的位置用O2
- 代替,下列对KO2晶体结构的描述正确的是
A.和K+距离相同且最近的O2 -共有8个
B.和K+距离相同且最近的K+共有12个
C.和K+距离相同且最近的O2 –构成的多面体是正八面体
D.和K+距离相同且最近的O2 –构成的多面体是正六面体
第Ⅱ卷(非选择题 共86分)
15.X元素的原子的最外层电子数与次外层电子数的差值等于电子层数。Y元素最外层电子比X元素的最外层电子多2个,则X与Y形成的化合物为
A、X3Y2 B、X2Y C、XY2 D、XY3
14.下列离子方程式中正确的是 ( )
A.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全
|
B.用惰性电极电解MgCl2溶液:2Cl-+2H2O 2OH-+H2↑+Cl2↑
C.三氯化铝溶液跟过量氨水反应:Al3++3NH3·H2O Al (OH)3↓+3NH4+
D.铜片投入稀HNO3溶液:Cu + NO3-+ 4H+ = Cu2+ + 2H2O + NO↑
13.在合成氨反应中,开始充入a mol N2和b mol H2,在一定条件下,反应达到平衡,测得NH3占混合气体的25%,则平衡时N2的转化率是
A、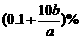 B、0.1(a+b) C、33.3% D、
B、0.1(a+b) C、33.3% D、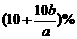
12.几种短周期元素的原子半径及主要化合价见下表:
|
元素代号 |
L |
M |
Q |
R |
T |
|
原子半径/nm |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
|
主要化合价 |
+2 |
+3 |
+6、-2 |
+2 |
-2 |
下列叙述正确的是
A.L、M的单质与稀盐酸反应速率L>M B.M与T形成的化合物有两性
C.Q、T两元素的氢化物分子间存在氢键 D.L、Q形成的简单离子核外电子数相等
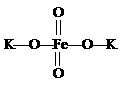
11.高铁酸钾 (K2FeO4)是一种新型、高效、多功能水处理剂,
是比Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染的绿色处理剂。工业是先制得高铁酸钠,然后在低温下,在高铁酸钠溶液中湿法制备的主要反应方程为:2Fe(OH)3+3ClO-+4OH-===2FeO42-+3Cl-+5H2O
干法制备的主要反应为:2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑
下列有关说法不正确的是
A.高铁酸钾中铁显+3价 B .湿法中每生成1 mol Na2FeO4转移3 mol电子
C.干法中每生成1 mol Na2FeO4转移4 mol电子
D.K2FeO4处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3等,生成的Fe(OH)3还能吸附水中的悬浮杂质
10.假定把12C的相对原子质量定为24,把24g12C含有的原子个数定为阿伏加德罗常数,而物质的量的概念不变。则下列推断不正确的是 A.此时16O的相对原子质量为32 B.标准状况下,44gCO2的体积为11.2L C.40gNaOH溶于水配成1L溶液,其物质的量浓度为1mol·L-1 D.44gCO2和28gCO含有相同数目的分子
9、科学家研制出多种新型杀虫剂,以代替DDT,化合物A是其中一种。下列关于这种化合物的说法正确的是
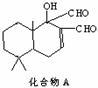 A.化合物A的化学式为C15H22O3
A.化合物A的化学式为C15H22O3
B.化合物A是芳香族化合物
C.化合物A可以发生卤代反应、酯化反应和银镜反应
D.1mol化合物A最多可与1molH2发生加成反应
8.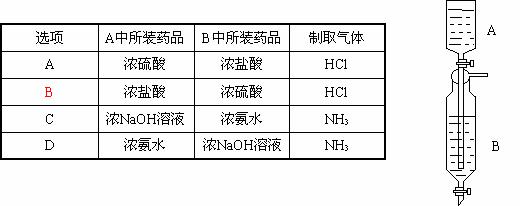 Inorganic Syntheses一书中,有一如图所示的装置,用以制备少量某种干燥的纯净气体。该装置中所装的药品正确的是
Inorganic Syntheses一书中,有一如图所示的装置,用以制备少量某种干燥的纯净气体。该装置中所装的药品正确的是
7.下列说法或表示正确的是
A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由单质A转化为单质B是一个吸热过程,由于可知单质B比单质A稳定
C.稀溶液中:H+(aq)+OH-(aq)  H2O(l); △H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含l mol NaOH的溶液混合,放出的热量大于57.3kJ
H2O(l); △H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含l mol NaOH的溶液混合,放出的热量大于57.3kJ
D.在101kPa时,H2燃烧的热化学方程式为:2H2(g)+O2(g) = 2H2O(l);
△H=-571.6kJ/mol,则H2在101kPa时的燃烧热为571.6kJ/mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com