
题目列表(包括答案和解析)
20.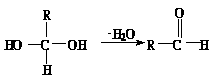 (13分)已知一个碳原子上连有两个羟基时,易发生下列转化:
(13分)已知一个碳原子上连有两个羟基时,易发生下列转化:
请根据下图回答。
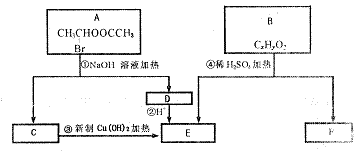 (1)E中含有官能团的名称是
;③的反应类型是
,C跟新制的氢氧化铜反应的化学方程化为
;
(1)E中含有官能团的名称是
;③的反应类型是
,C跟新制的氢氧化铜反应的化学方程化为
;
(2)已知B的相对分子质量为162,其燃烧产物中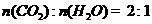 则B的分子式为
,F的分子式为
。
则B的分子式为
,F的分子式为
。
(3)在电脑芯片生产领域,高分子光阻剂是光刻蚀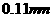 线宽芯片的关键技术。F是这种高分子光阻剂生产中的主要原料。F具有如下特点:①能跟
线宽芯片的关键技术。F是这种高分子光阻剂生产中的主要原料。F具有如下特点:①能跟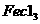 溶液发生显色反应:②能发生加聚反应;③芳环上的一氯代物只有两种。F在一定条件下发生加聚反应的化学方程式为
。
溶液发生显色反应:②能发生加聚反应;③芳环上的一氯代物只有两种。F在一定条件下发生加聚反应的化学方程式为
。
(4)化合物G是F的同分异构体,它属于芳香族化合物,能发生银镜反应。G可能有
种结构,写出其中任一种同分异构体的结构简式 。
19.(12分)现有中学常见的三种单质甲、乙、丙,它们在一定条件下会发生如下变化,其中次要生成物已略去。
(1)已知乙元素的+2价离子与Ne原子具有相同的电子层结构,则②的离子方程式为 ,④化学方程式为 ;
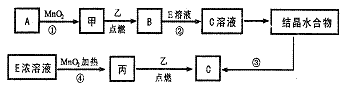 (2)若反应①可在常温下进行,则A的名称是
。若反应①需在加热条件下进行,则A的名称是
,反应的化学方程式为
;
(2)若反应①可在常温下进行,则A的名称是
。若反应①需在加热条件下进行,则A的名称是
,反应的化学方程式为
;
(3)从C溶液中得到C需经过两步操作:先从C溶液中得到晶体,再将得到的晶体转化为C。从C溶液中得到晶体的过程被称为 ,将得到的晶体转化为C的实验条件是 。
18.(13分)工业上用固体硫酸亚铁制取颜料铁红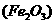 ,反应原理是:
,反应原理是: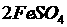
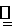
 。某研究性学习小组用下图所示装置分别检验该反应所产生的气态物质,然后利用装A瓶内的生成物来测定已分解的
。某研究性学习小组用下图所示装置分别检验该反应所产生的气态物质,然后利用装A瓶内的生成物来测定已分解的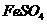 的质量。(已 知
的质量。(已 知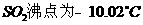 )
)
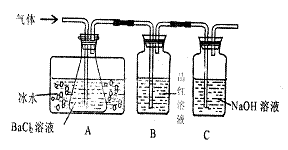 请回答相关问题:
请回答相关问题:
(1)本实验中,A瓶所盛BaCl2:溶液可以吸收的气体是 ,发生反应的离子方程式为 。
(2)A瓶所盛的试剂的作用是 ;C瓶所盛试剂的作用是 。
(3)A瓶要用冷水冷却的原因是
.
(4)某学生欲利用装置B反应前后质量差确定已分解的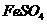 质量,你认为该同学方案是否合理 (填“合理”、“不合理”),理由是
质量,你认为该同学方案是否合理 (填“合理”、“不合理”),理由是
。
(5)依据上述装置和反应事实,请设计测定己分解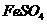 质量的操作和方法:
质量的操作和方法:
。
17. (7分)右图足化学实验中出现频率较高的装置,它是由物质制备和检验生成物性质两部分组成的(暂不考虑除杂、尾气的吸收),请你选用中学化学常见试剂设计一个实验,通过乙中的反应和丙中的实验现象,得出三种物质性质递变的结沦。将所用试剂名称、丙中现象及由此得出的实验结论填入下列空白处:
(7分)右图足化学实验中出现频率较高的装置,它是由物质制备和检验生成物性质两部分组成的(暂不考虑除杂、尾气的吸收),请你选用中学化学常见试剂设计一个实验,通过乙中的反应和丙中的实验现象,得出三种物质性质递变的结沦。将所用试剂名称、丙中现象及由此得出的实验结论填入下列空白处:
所用试剂:甲 、乙 、丙 。
丙中现象: 。
实验结论: 。
16.已知某温度、压强下的气体摩尔体积为 ,在该条件下有
,在该条件下有 气体X发生如下反应并达到平衡;
气体X发生如下反应并达到平衡;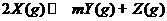 ,测得混合气体中X的体积分数为58.80%,混合气体的总质量为
,测得混合气体中X的体积分数为58.80%,混合气体的总质量为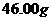 ,混合气体的的密度为
,混合气体的的密度为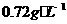 。则平衡混合气体的平均相对分子质量为
。则平衡混合气体的平均相对分子质量为
A.58.80 B.46.00 C.39.74 D.16.13
第Ⅰ卷答 题 栏
得分栏
第Ⅱ卷(非选择题 共62分)
本卷包括6道题,共62分。
15.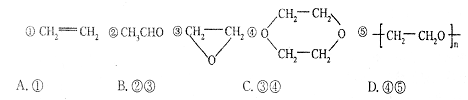 已知乙烯醇
已知乙烯醇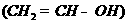 不稳定,可自动转化为乙醛。乙二醇在一定条件下发生脱水反应,也有类似现象发生,所得产物的结构筒式有人写出下列几种,其中不可能的是
不稳定,可自动转化为乙醛。乙二醇在一定条件下发生脱水反应,也有类似现象发生,所得产物的结构筒式有人写出下列几种,其中不可能的是
14.下列离子方程式正确的是
A.水中加入过氧化钠固体: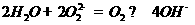
B.等物质的量的氢氧化钡溶液与明矾溶液混合
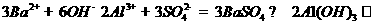
C.氢氧化镁与稀硫酸反应: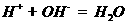
D.单质铜与稀硝酸反应: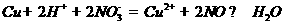
13.在如图所示的装置中,烧瓶中盛有空气,广口瓶中盛放下列物质时可发生喷泉的选项是
A.块状大理石和稀硫酸 B.NH4Cl与稀NaOH溶液
C.Na2O2与NaOH溶液 D.铜片与稀盐酸
12.在一定温度下,某浓度的硝酸与金属锌反应生成NO2和NO的物质的量之比为1:3,则要 使1 mol金属锌完全反应,需要硝酸的物质的量为
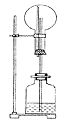 A.2.8 mol B.2.6 mol C.2.4
mol D.0.8mol
A.2.8 mol B.2.6 mol C.2.4
mol D.0.8mol
11.在一定温度下,物质M的溶解度为Ag。向(100+A)g物质M的饱和溶液中加入A g M,析出带一定结晶水的晶体B g,现取出B g结晶水合物加水配成相同温度下的饱和溶液,需加水的质量为
A.100 g B.大于100 g C.小于100 g D.(100+A) g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com