
题目列表(包括答案和解析)
17.如图中的虚线上方空间有垂直线框平面的匀强磁场,直角扇形导线框绕垂直于线框平面的轴O以角速度ω匀速转动.设线框中感应电流方向以逆时针为正方向,那么在图中能正确描述线框从图所示位置开始转动一周的过程中,线框内感应电流随时间变化情况的是

16.我们的银河系的恒星中大约四分之一是双星.某双星由质量不等的星体s1和s2构成,两星在相互之间的万有引力作用下绕两者连线上某一定点c做匀速圆周运动,由天文观察测得其运动周期为T,s1到c点的距离为r1,s1和s2的距离为r,已知引力常量为G,由此可求出s2的质量为


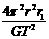
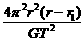
A. B. C. D.
15.下列说法正确的是
A.热量不能由低温物体传递到高温物体
B.外界对物体做功,物体的内能必定增加
C.第二类永动机不可能制成,是因为违反了能量守恒定律
D.不可能从单一热源吸收热量并把它全部用来做功,而不引起其他变化
14. 氦原子被电离一个核外电子,形成类氢结构的氦离子。已知基态的
氦原子被电离一个核外电子,形成类氢结构的氦离子。已知基态的
氦离子能量为E1=-54.4eV,氦离子能级的示意图如图所示。在具有
下列能量的光子中,不能被基态氦离子吸收而发生跃迁的是
A.40.8eV B.43.2eV
C.51.0eV D.54.4eV
13.将一定量的Fe、Fe2O3、CuO的混合物加入到100ml 2.2mol·L-1 H2SO4溶液中,充分反应后,生成的气体在标准状况下为896ml,得到不溶固体1.28g,过滤后,往滤液中滴加几滴KSCN溶液,不变红(假设滤液体积仍为100ml),向滤液中滴加2mol·L-1 NaOH溶液,至40ml时才开始出现沉淀,则未滴加NaOH溶液前滤液中FeSO4的物质的量浓度为
A.1.7mol·L-1 B.1.8mol·L-1 C.1.9mol·L-1 D.2.0mol·L-1
12. 萤火虫体内发光的物质是萤光素,其结构式为:
萤火虫体内发光的物质是萤光素,其结构式为:
下列有关萤光素的说法正确的是
A.它的分子式为C11H7O3N2S2
B.萤光素溶液与FeCl3溶液能发生显色反应
C.在Ni作催化剂下,1mol萤光素最多能与3molH2发生加成反应
D.1mol萤光素能与1mol Na2CO3溶液反应
11. 常温常压下,注射器甲中装有NO2气体,注射器乙中装有相同
常温常压下,注射器甲中装有NO2气体,注射器乙中装有相同
体积的空气,注射器与U形管连通,如图所示,打开两个止水
夹,同时向外拉两注射器的活塞,且拉动的距离相等,将会看
到U形管中液面(不考虑此条件下NO2与水的反应)
A.a端上升,b端下降
B.a端下降,b端上升
C.U形管中液面无变化
D.无法判断
10. 现有pH=2的A、B两种酸溶液各lmL,分别加水稀释到1L,其pH
现有pH=2的A、B两种酸溶液各lmL,分别加水稀释到1L,其pH
与溶液体积的关系如图所示,下列说法正确的是
①a=5时,A是强酸,B是弱酸
②稀释后,A溶液的酸性比B溶液强
③若A、B均为弱酸,则2<a<5
④若A、B均为强酸,则A、B的物质的量浓度一定相等
A.①② B.①③ C.①③④ D.②③④
8.将一定量的五氟化碘(IF5)与水反应生成碘酸和氟化氢(IF5+3H2O=HIO3+5HF),生成的碘酸在弱酸性溶液中与KI反应生成单质I2(IO3-+5I-+6H+=3I2+3H2O),现用标准的硫代硫酸钠滴定I2(2Na2S2O3+I2=Na2S4O6+2NaI),若消耗Na2S2O3 0.3mol,则IF5的物质的量为
A.0.1mol B.0.2mol C.0.3mol D.0.05mol
 9.往一体积不变的密闭容器中充入H2和I2,发生反应:H2(g)+I2(g)
9.往一体积不变的密闭容器中充入H2和I2,发生反应:H2(g)+I2(g)
?2HI(g);ΔH<0,当达到平衡后,改变反应的某一条件(不再充入
任何气体),造成容器内压强增大,下列说法正确的是
A.容器内气体颜色变深,平均相对分子质量增大
B.平衡向右移动,HI浓度增大
C.改变条件前后,速率图象如右图
D.平衡不移动,混合气体密度不变
7.下列离子反应方程式正确的是
A.在Ba(OH)2溶液中加入少量的NaHSO4溶液:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
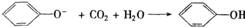 B.NH4HSO3与足量的NaOH溶液反应:HSO3-+OH-=SO32-+H2O
B.NH4HSO3与足量的NaOH溶液反应:HSO3-+OH-=SO32-+H2O
C.向苯酚钠溶液中通人少量的CO2气体: +HCO3-
D.标准状况下,将112ml C12缓慢通人10ml 1mol·L-1FeBr2溶液中:2Fe2+ +4Br-+3C12= 2Fe3++6C1-+2Br2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com