
题目列表(包括答案和解析)
17.分子量为M的某物质在室温下的溶解度为Sg/100g水,此时测得饱和溶液的密度为dg/cm3。则该饱和溶液的物质的量浓度是 ( )
A. mol·L-1 B.
mol·L-1 B. mol·L-1
mol·L-1
C. mol·L-1 D.
mol·L-1 D. mol·L-1
mol·L-1
16.在标准状况下,将VLA气体(摩尔质量为Mg/mol)溶于0.1L水中,所得溶液密度为dg/mL,则此溶液的物质的量浓度为( )mol/L。
A. B.
B.
C.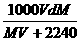 D.
D.
15.据最新报道,科学家发现了如下反应:O2+PtF6=O2(PtF6),已知O2(PtF6)为离子化合物,其中Pt为+5价,对于此反应,下列说法正确的是 ( )
A.在此反应中,O2是氧化剂,PtF6是还原剂
B.O2(PtF6)中氧元素的化合价是+1价
C.O2(PtF6)中不存在共价键
D.在此反应中,每生成1 mol O2(PtF6),则转移1 mol电子
14.用NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
A.常温常压下乙炔的1,3-丁二烯混合气ag,其中C-H键的数目约为aNA/13
B.工业生产硫酸时,在接触室内每充入NA个SO2可完全转化为1 molSO3
C.1 mol干冰晶体中含有C=O键的数目为2NA
D.1 molCa(ClO)2只作氧化剂且充分反应时,转移的电子数一定为2NA
13.下列说法中,正确的是 ( )
A.在100g水里,最多能溶解36g食盐,所以食盐的溶解度为36g
B.所有固体物质溶解度都随着温度的升高而增大
C.有过剩溶质与溶液共存的溶液一定是该温度时的饱和溶液
D.20℃时100g水里溶解了30g硝酸钾,所以硝酸钾的溶解度是30g
12.下列有关物质的结构或性质的叙述错误的是 ( )
A.由极性键形成的分子不一定是极性分子
B.水是一种非常稳定的化合物,这是由于氢键所致
C.石英、食盐、金属钠、干冰的熔点依次降低
D.分子晶体中一定存在分子间作用力,可能有共价键
11.将SO2通入BaCl2溶液至饱和,未见沉淀生成,继续通入另一种气体,仍无沉淀,则通入的气体可能是 ( )
A.CO2 B.NH3 C.NO2 D.H2S
10.将甲、乙两种金属的性质相比较,已知①甲跟H2O反应比乙与H2O反应剧烈;②甲单质能从乙的盐溶液中置换出单质乙;③甲的最高价氧化物的水化物碱性比乙的最高价氧化物的水化物碱性强;④与某金属反应时甲原子得电子数目比乙的多;⑤甲单质的熔、沸点比乙的低。能说明甲的金属性比乙强的是 ( )
A.①④ B.③⑤ C.①②③ D.①②③④⑤
8.有Na2CO3、AgNO3、BaCl2、HCl、NH4NO3 5瓶无标签的溶液,为鉴别它们,取4支试管分别装入一种溶液,再向上述4支试管中加入少许剩下的一种溶液,下列表达中错误的是 ( )
A.若3支试管出现沉淀时,则后加入的是AgNO3溶液
B.若全部没有什么现象变化时,后加的是NH4NO3溶液
C.若1支试管出现气体,2支试管出现沉淀时,最后加入的是HCl溶液
D.若只有2支试管出现沉淀其他试管均无明显现象时,则后加的是BaCl2溶液
|
A.用盐析的方法,提纯某些蛋白质
B.用渗析的方法,除去淀粉溶液中的N aCl
C.用蒸馏的方法,分离乙酸乙酯和乙酸钠溶液
D.用过滤的方法,分离出饱和碳酸钠溶液与过量的CO2反应后的产物
7.下列对物质用途的描述中,错误的是 ( )
A.漂粉精及明矾都可作自来水的消毒剂
B.二氧化硫可用来漂白纸浆、毛、丝等
C.重晶石常作X射线透视肠胃的“钡餐”
D.铝可用于冶炼某些熔点较高的金属
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com