
题目列表(包括答案和解析)
5.下列各组离子在溶液中能大量共存,当加入过量氨水后也不产生沉淀的是 ( )
A.Na+、Ba2+、Cl-、SO42- B.K+、AlO2-、NO3-、OH-
C.H+、NH4+、Al3+、SO42- D.H+、Cl-、CH3COO-、NO3-
4.限用硫酸、盐酸、醋酸、钠盐、钾盐、钡盐相互反应,符合离子方程式2H++SO32-=H2O+SO2的化学方程式个数的是 ( )
A.4 B.5 C.8 D.12
3.下列盐溶液中,加入BaCl2溶液后有白色沉淀生成,再加入稀硝酸,白色沉淀不消失的是 ( )
A.NaHCO3 B.Na2CO3 C.Na2SO4 D.Na3PO4
2.在下列反应中水既不是氧化剂,又不是还原剂的氧化还原反应是 ( )
A.氟气溶于水 B.金属钠溶于水
C.过氧化钠溶于水 D.五氧化二磷溶于热水
1.为维持人体内电解质平衡,人在大量出汗后应及时补充的离子是 ( )
A.Mg2+ B.Ca2+ C.Na+ D.Fe3+
23、YBa2Cu3Ox是近年来科学家发现的一种高温超导材料(属非整比化合物)。YBa2Cu3Ox中,Y、Ba、O三种元素都有固定的化合价,分别为+3、+2、-2,而Cu是+2和+3的混合价态,化学式中x为未知数。现用碘量法测Cu,进而求得x值。
取4.00×10-2g YBa2Cu3Ox样品,用稀盐酸溶解,在氩气保护下加1gKI固体。样品中的Cu3+和Cu2+分别氧化KI,再用0.0100mol/LNa2S2O3溶液滴定得到I2(Cu3++3I-=CuI+I2,2Cu2++4I-=2CuI+I2),终点时消耗Na2S2O3溶液23.45mL。另取一份质量相等的YBa2Cu3Ox样品,用稀盐酸溶解,煮沸,使其中的Cu3+全部转化为Cu2+,冷却后用碘量法滴定,终点时消耗18.13mL 0.0100 mol/L Na2S2O3(在滴定时S2O32-转变为S4O62-)。请回答下列问题:
(1) 写出在滴定过程中S2O32转变为S4O62--离子方程式。
(2) 求出Cu3+和Cu2-物质的量之比。
29.I.恒温、恒压下,在一个可变容积的容器中发生如下发应:
A(气)+B(气) C(气)
C(气)
(1)若开始时放入1molA和1molB,到达平衡后,生成a molC,这时A的物质的量为 mol。
(2)若开始时放入3molA和3molB,到达平衡后,生成C的物质的量为 mol。
(3)若开始时放入x molA,2molB和1molC,到达平衡后,A和C的物质的量分别是ymol和3a mol,则x= mol,y= mol。
平衡时,B的物质的量 (选填一个编号)
(甲)大于2 mol (乙)等于2 mol
(丙)小于2 mol (丁)可能大于、等于或小于2mol
作出此判断的理由是 。
(4)若在(3)的平衡混合物中再加入3molC,待再次到达平衡后,C的物质的量分数是 。
II.若维持温度不变,在一个与(1)反应前起始体积相同、且容积固定的容器中发生上述反应。
(5)开始时放入1molA和1molB到达平衡后生成b molC。将b与(1)小题中的a进行比较 (选填一个编号)。
(甲)a<b (乙)a>b (丙)a=b (丁)不能比较a和b的大小
作出此判断的理由是 。
28.某学生用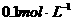 的
的 标准溶液滴定未知浓度盐酸,其操作可分解为如下几步:
标准溶液滴定未知浓度盐酸,其操作可分解为如下几步:
A. 移取 待测盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
待测盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
B. 用标准溶液润洗滴定管2-3次
C. 把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D. 取标准 溶液注入碱式滴定管至刻度0以上2-3厘米
溶液注入碱式滴定管至刻度0以上2-3厘米
E. 调节液面至0或0以下刻度,记下读数
F. 把锥形瓶放在滴定管的下面,用标准 溶液滴定至终点并记下滴定管液面的刻度。就此实验完成填空:
溶液滴定至终点并记下滴定管液面的刻度。就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)____________________________。
(2)上述B步骤操作的目的是____________________。
(3)上述A步骤操作之前,先用待测溶液润洗锥形瓶,则对滴定结果的影响是________。
(4)判断到达滴定终点的实验现象是___________________________。
(5)若称量一定量的 固体(含少量
固体(含少量 )配制标准溶液并用来滴定上述盐酸则对滴定结果的影响是_________________________________________。
)配制标准溶液并用来滴定上述盐酸则对滴定结果的影响是_________________________________________。
27、从某些方面看,氨和水相当。试回答:
(1)氮可形成多种离子,其中N2H5+ 、N2H62+是由中性分子结合质子形成的(类似NH4+)。因此有类似于NH4+的性质,试写出N2H62+在强碱性溶液中反应的离子方程式 。
(2)若液氨相当于地球上的水以满足木星上生物生活的需要,假若那里的生命分子也是以碳链为骨架的话,那么木星上生物体内与地球上生物中葡萄糖的分子结构相当的化合物是
。(写结构简式)。
(3)有A、B、C、D、E五种气体,C对空气的相对密度为2.45,在相同温度和压力下,B、D、E的密度之比为4︰2︰1,这五种气体均为常见气体,各气体两两混合时出现如下情况:
|
气体 |
A+B |
A+E |
C+E |
D+E |
B+C |
|
反应情况 |
不用光照能反应 |
不反应 |
漫射光下反应 |
点燃反应 |
有水存在时易反应 |
据此可以推知:(填化学式)
A ,B ,C ,D ,E 。
26.根据下列反应框图填空,已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应。
(1)单质L是 。
(2)化合物B是 。
(3)图中除反应①以外,还有两个用于工业生产的反应,是 和 (填代号)。
它们的化学反应方程式分别是 和 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com