
题目列表(包括答案和解析)
21.(共14分)下图所示是进行木炭与浓硝酸反应,并检验生成的气体和反应的热效应的实验装置,它具有无污染,现象明显的特点。具支试管A中所盛固体下层是无水CaCl2(作载体不参加反应),上层是红热的木炭。实验时慢慢将浓硝酸滴到木炭上,反应即开始进行且能长时间剧烈反应。请回答下列问题:
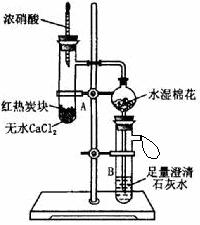
(1)写出木炭与浓硝酸反应的化学方程式_____________________________。
(2)该反应的反应热△H________________0(填“>”或“<”),这一结论的实验证据是____________________________________________________。
(3)实验中具支试管A内出现的现象是____________________________。
(4)试管B内出现的现象为 ;澄清石灰水中发生的主要反应的离子方程式为_______________________________________。
(5)某学生在实验临近结束时,发现滴管中的浓硝酸难以滴下。若要再滴入几滴浓硝酸使木炭反应完全,最简单的办法是 。
20.(共10分)如下图所示,A溶液呈蓝色。(图中参加反应的水及生成的水已略去)
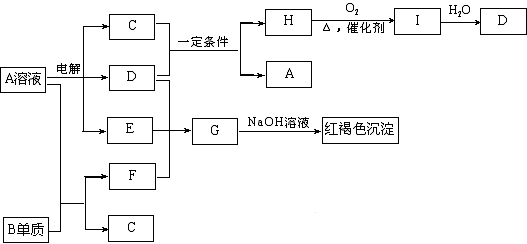
请回答下列问题:
(1)写出电解A溶液的离子方程式: ;
(2)写出C和D在一定条件下反应的化学方程式: ;
(3)写出G的化学式: ;
(4)若欲将A溶液与B单质反应的化学能转化为电能,则所设计的原电池的正极材料可以是: ;负极的反应式是: 。
19.(共12分)某无色溶液,其中可能存在Na+、Ba2+、AlO2-、S2-、SO32-、SO42-;取该溶液进行有关实验,实验结果如下图所示。

请回答下列问题:
(1)沉淀甲的化学式为 ;
(2)由溶液甲生成沉淀乙的离子方程式为 ;
(3)沉淀丙中一定含有 ,可能含有 ;
(4)综合上述信息,该溶液中肯定存在的离子有 。
18.(共8分)运载宇宙飞船的火箭燃料除液态双氧水外,还有另一种液态化合物N2H4。请回答下列问题:
(1)化合物N2H4的电子式为 ,
(2)若8g液态化合物N2H4与液态双氧水恰好完全反应,产生两种无毒且不污染环境的气态物质,并放出375kJ的热量。写出该反应的热化学方程式:
。
(3)任写出两种与N2H4等电子数的氢化物的分子式__________、__________。
17.(共8分)晶态氯化钠是____ _晶体。晶体中,每个钠离子周围有_ _ _个氯离子,每个氯离子周围有__ __个钠离子,钠离子半径比氯离子半径 。在氯化物MCl中,M在第六周期,是钠的同族元素,该晶体中每个阳离子周围有____个氯离子。钠的金属性比M_ 。氯化钠的电子式是_____,熔融后______电(导或不导)。
16.将3.48g四氧化三铁完全溶解在100ml 1mol/L硫酸中,然后加入25ml.K2Cr2O7溶液,恰好使溶液中Fe2+全部转化为Fe3+,Cr2O72-离子全部还原为Cr3+.则K2Cr2O7溶液的物质的量浓度为
A.0.05mol/L B.0.10mol/L C.0.15mol/L D.0.20mol/L
Ⅱ卷(非选择题 共62 分)
15.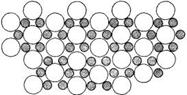 今年3月发现硼化镁在39 K呈超导性,可能是人
今年3月发现硼化镁在39 K呈超导性,可能是人
类对超导认识的新里程碑。在硼化镁晶体的理想模
型中,镁原子和硼原子是分层排布的,一层镁一层
硼的相间排列,右图是该晶体微观空间中取出的部
分原子沿Z轴方向的投影,白球是镁原子投影,黑
球是硼原子投影,图中的硼原子和镁原子投影在同
一平面上。可确定硼化镁的化学式为
A.MgB B.MgB2 C.Mg2B D.MgB6
14.下列叙述不正确的是
A.电解时在阴极上发生还原反应
B.电镀时,阳极材料发生氧化反应
C.电解饱和食盐水时,阴极区产物为氢氧化钠溶液和氢气
D.原电池跟电解池连接后,电子从原电池负极流向电解池阳极
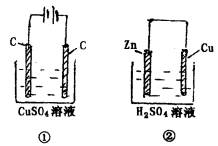
13.电解质溶液的浓度均为0.1mol·L-1,
工作一段时间后,测得导线上都通过
了0.02 mol e-,若不考虑溶液体积的变
化,则下列叙述正确的是
A.产生气体体积:①=②
B.电极上析出固体质量:①<②
C.电极反应式:①中阳极:4OH――4e-=2H2O+O2↑ ②中负极:2H++2e-=2H2↑
D.溶液的pH变化:①减小;②增大
12.在工业上制造硫酸的生产过程中,按反应的先后顺序依次使用的主要设备是
A.沸腾炉、吸收塔、热交换器 B.热交换器、沸腾炉、接触室
C.沸腾炉、接触室、吸收塔 D.沸腾炉、吸收塔、接触室
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com