
题目列表(包括答案和解析)
6、下列各组物质相互作用时:反应物的量或外界条件的改变,不会引起产物种类改变的是( )
A、Na和O2 B、NaOH溶液和CO2
C、Na2O2和CO2 D、Ca(OH)2溶液和小苏打溶液
5、下列叙述正确的是 ( )
A、离子晶体中,只存在离子键,不可能存在其它化学键
B、在卤族元素(F、Cl、Br、I)的氢化物中,HF的沸点最低
C、NaHSO4、Na2O2晶体中的阴阳离子个数比均为1∶2
D、晶体熔点:金刚石>食盐>冰>干冰
4、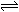 在一密封烧瓶中注入NO2,25℃时建立下列平衡;2NO2 N2O4;△H<0,把烧瓶置于100℃沸水中,下列情况不变的是
( )
在一密封烧瓶中注入NO2,25℃时建立下列平衡;2NO2 N2O4;△H<0,把烧瓶置于100℃沸水中,下列情况不变的是
( )
①颜色 ②平均相对分子质量 ③质量 ④压强 ⑤密度
A、③⑤ B、①④ C、②③⑤ D、③④⑤
3、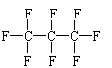 最近美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳有效104倍的超级温室气体--全氟丙烷(C3F8),并提出用其“温室化火星”,使火星成为第二个地球的计划。有关全氟丙烷的说法不正确的是
( )
最近美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳有效104倍的超级温室气体--全氟丙烷(C3F8),并提出用其“温室化火星”,使火星成为第二个地球的计划。有关全氟丙烷的说法不正确的是
( )
A、分子中三个碳原子不可能处于同一直线上 B、全氟丙烷的结构式为
C、相同压强下,沸点:C3F8<C3H8
D、全氟丙烷分子中既有极性键,又有非极性键
2、今年7月28日上午8时45分,位于射阳县临海镇的氟源化工有限公司一车间突然发生爆炸,造成重大伤亡。给我们安全敲响了警钟。日常生活中的下列做法存在安全隐患的是( )
①机动车推广使用乙醇汽油;②液化石油气罐中残留液体倒入下水道;③为降低居室甲醛含量,新装修住房应紧闭门窗,并放置一盆水;④虾仁等水产品用甲醛的稀溶液进行处理,延长保鲜时间;⑤节日大量燃发烟花爆竹,增加喜庆气氛。
A、全部 B、除①外 C、除①③外 D、除③⑤外
1、“信息”“材料”“能源”被称为新科技革命的三大支柱。下列有关资讯错误的是 ( )
A、在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源
B、目前中、美、日等国掌握的陶瓷发动机技术,大大提高了发动机的转化效率
C、合成高分子材料的广泛应用有百利而无一害
D、B4C3常用于制造切削工具和高温热交换器,它是一种新型无机非金属材料
24. (10分)有如下化学反应:2A(g)+B(g)
2C(g)(△H<0=
(10分)有如下化学反应:2A(g)+B(g)
2C(g)(△H<0=
(1)若将4mol气体A和2mol气体B在2L密闭容器中混合,经2s后测得C的浓度为0.6mol·L-1。则2秒时B的浓度为 mol·L-1。
(2)若把amol气体A和b mol气体B充入上述密闭容器,达到平衡时,它们的物质的量满足n(A)+n(B)=n(C),则气体A的转化率为 。
(3)如下图所示,将4mol气体A和2mol气体B混合后置于体积可变的等压容器中,一定温度下达到平衡状态X时,测得气体总物质的量为4.2mol。若A、B、C起始的物质的量分别用a、b、c表示,试回答:
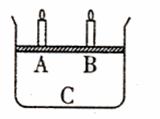
ⅰ:达到平衡状态X时的容器中,通入少量B气体,容器中A的体积分数 (填“增大”、“减小”或“不变”)。若要使A的体积分数再升高到与平衡状态X相同,可采取的一种措施是 (只填一种即可)。
ⅱ:若起始a=1.2mol,b=0.6mol,且达到平衡后各气体的体积分数与平衡状态X相同,则起始时C的取值范围为 。
23. (10分)已知:Ⅰ.CH3COONa+NaOH
CH4↑+Na2CO3
(10分)已知:Ⅰ.CH3COONa+NaOH
CH4↑+Na2CO3
|
 Ⅱ.R-CH==CH2+H2O
RCH2CH2OH
Ⅱ.R-CH==CH2+H2O
RCH2CH2OH
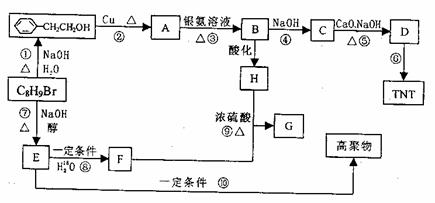 现有分子式C8H9Br的有机物在一定条件下能发生下图所示的一系列反应:
现有分子式C8H9Br的有机物在一定条件下能发生下图所示的一系列反应:
请回答下列问题:
(1)写出C8H9Br的结构简式: 。
(2)上述反应中属于消去反应的有(填编号) 反应。
(3)写出反应⑥、⑨的化学方程式:
反应⑥:
反应⑨:
(4)写出H可能有的3种同分异构体(要求:a.苯环上只有一个取代基,b.3种异构体不同类别):
22.(16分)某无色溶液中可能存在的离子如下: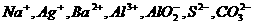
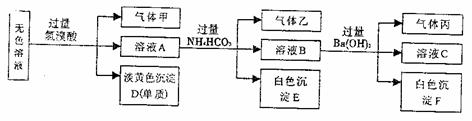
 。取10mL该溶液进行实验,有关实验过程、现象及产物如下图所示:
。取10mL该溶液进行实验,有关实验过程、现象及产物如下图所示:
回答下列问题:
(1)沉淀D是(填名称) ,生成该沉淀的离子方程式为:
;
生成气体乙的离子方程式为: ;
生成沉淀F的离子方程式为: ;
(2)若测知气体甲为两种成分,则气体和原溶液中溶质的可能组成为(将结果填入下表中。)
|
可能情况 |
(1) |
(2) |
|
气体可能 组成 |
|
|
|
溶质可能组成 (填化学式) |
|
|
(3)若测知气体甲的成分只有一种时,则原溶液中一定存在的离子有 ,可能存在的离子有 。
|
21.(12分)某课外兴趣小组为了探究铁与硫在隔绝空气的条件下反应所得固体M的成分,设计了下图所示装置。打开分液漏斗D中活塞,缓慢加入稀盐酸至过量,与固体M充分反应。待反应停止后,B中有黑色沉淀析出,C中量气装置右边液面上升,调节量气装置使左右液面相平后,测得进入C中的气体为V mL(已换算成标准状况)。
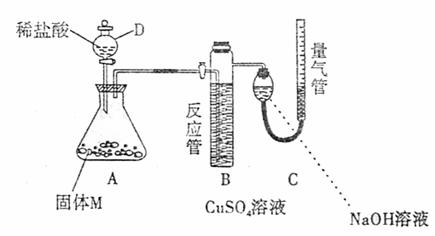
根据上述实验事实,回答下列问题:
(1)加入药品和实验开始前必须进行的操作是 。
(2)固体M中一定有的物质是 (写化学式)。
(3)写出A中发生反应的化学方程式(只写一个):
。
(4)写出B中析出黑色沉淀时发生反应的离子方程式 。
(5)根据题给条件,固体M中一种物质的质量可以确定,应为 g(用代数式表示)。
(6)稀盐酸与固体M反应后还残留淡黄色固体,该固体可能是 (写化学式),要分离该固体,在实验操作中,除烧杯、玻璃棒外,还需要的玻璃仪器是 。
(7)反应完成后,取A中溶液少许加入试管中,要确定固体M中是否含有Fe3+,需加入的试剂为: 。
A.KSCN溶液 B.NaOH溶液 C.氨水
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com