
题目列表(包括答案和解析)
8、下列说法或表示方法中正确的是
A、在稀溶液中,H+(aq)+OH-(aq)=H2O(1);△H=-57.3kJ·mol-1,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热大于57.3kJ
B、由C(石墨)=C(金刚石);△H=+1.90kJ·mol-1可知,金刚石比石墨稳定
C、等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
D、在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(g)=2H2O(1);△H=-285.8kJ·mol-1
7、下列说法中不正确的是
A、在金刚石晶体中最小的碳原子环上有6个碳原子
B、在氯化铯晶体中每一个Cs+ 周围与其等距离且最近的Cl- 有8个
C、在氯化钠晶体中每一个Na+ 周围与其等距离且最近的Na+ 有12个
D、水是一种非常稳定的化合物,这是由于水分子间能形成氢键的缘故
6、原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关,下列说法不正确的是
A、由Al、Cu、稀H2SO4组成原电池,其负极反应式为:Al-3e-=Al3+
B、由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+4OH-=AlO2-+2H2O
C、由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu-2e-=Cu2+
D、由Al、Cu、浓硝酸组成原电池,其负极反应式为:Cu-2e-=Cu2+
5、下列工业生产的说法错误的是
A、氯碱工业中隔离两电极的材料是阳离子交换膜,因此该生产工艺又称“阳离子交换膜法”
B、石膏可作为生产硫酸的原料之一
C、由于常压下SO2转化为SO3的转化率很高,所以SO2接触氧化时不采用高压的反应条件
D、合成氨的反应是放热反应,因此工业上合成氨常采用低温条件
4、下列实验操作能达到测量要求的是
A、用托盘天平称量25.20g氯化钠 B、用10mL量筒量取7.50mL稀硫酸
C、用25mL滴定管量取14.80mL溶液 D、用广泛pH试纸测得溶液的pH为4.2
3、时下,一种被称为“魔棒”的荧光棒已成为节日之夜青少年的喜爱之物,其发光原理是利用过氧化氢氧化草酸酯产生能量,该能量被传递给荧光物质后便发生荧光。下列有关叙述中不正确的是
A、草酸酯中混有的草酸可用饱和碳酸钠溶液除去
B、草酸能使蓝墨水褪色
C、草酸受热时分解出来的气体产物是混合物
D、“魔棒”不能接近石油气之类的可燃性气体,否则可能会导致爆炸
1、近代10大科技突破中“火星上‘找’到水的影子”名列第一。下列说法中错误的是
A、用离子交换法可以使海水淡化
B、使用高效催化剂可使水分解,同时释放能量
C、4℃时水的密度最大,对水生动植物的生命活动有重大意义
D、水是金属发生电化学腐蚀的主要因素之一
|
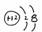 A、镁离子结构示意图
B、羟基电子式 H
A、镁离子结构示意图
B、羟基电子式 H

|
|
C、次氯酸电子式H D、氨分子结构
25.(8分)将铁粉与氧化铁的混合物19.2g,加入200mL稀H2SO4,放出3360mL氢体(标况),反应后溶液中无固体剩余。向反应后的溶液里加入KSCN溶液,不呈血红色。中和过剩的酸,并将全部Fe2+沉淀为Fe(OH)2,共用去4mol/L NaOH溶液200mL。
求:
(1)原混合物中Fe2O3的质量分数;
23.(4分)FeCl3的浓溶液溶解铜粉的离子方程式为:2Fe3++Cu=2Fe2++Cu2+。现向FeCl3溶液中加入ag铜粉,搅拌使之全部溶解,再向其中加入bg铁粉,经充分反应后,过滤,得cg滤渣。若已知a>b>c,试推断滤渣是 ,滤液中的金属离子是 。
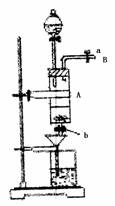 24.(12分)三氯化铁是中学化学实验室中必不可少的重要试剂。某同学利用废铁屑(含少量铜等不与盐酸反应的杂质)来制备FeCl3·6H2O,该同学设计的实验装置如右图所示,A中放有废铁屑,烧杯中盛有过量的稀硝酸,实验时打开a,关闭b,从分液漏斗内向A中滴加过量盐酸,YC此时溶液呈浅绿色,再打开b 进行过滤,过滤结束后,取烧杯内溶液倒入蒸发皿加热,蒸发掉部分开水并使多余HNO3分解,再降温结晶得FeCl3·6H2O晶体。请填写下列空白:
24.(12分)三氯化铁是中学化学实验室中必不可少的重要试剂。某同学利用废铁屑(含少量铜等不与盐酸反应的杂质)来制备FeCl3·6H2O,该同学设计的实验装置如右图所示,A中放有废铁屑,烧杯中盛有过量的稀硝酸,实验时打开a,关闭b,从分液漏斗内向A中滴加过量盐酸,YC此时溶液呈浅绿色,再打开b 进行过滤,过滤结束后,取烧杯内溶液倒入蒸发皿加热,蒸发掉部分开水并使多余HNO3分解,再降温结晶得FeCl3·6H2O晶体。请填写下列空白:
(1)从B导管收集产生的气体可采用的方法是 。
(2)滴加盐酸时,发现反应速率比盐酸与纯铁粉反应要快,
其原因是 。
(3)烧杯内放过量稀HNO3的原因是 ,
离子方程式是 。
(4)整个实验过程中,弹簧夹a都必须打开,除了为排出产生
的气体外,另一个目的是 。
(5)用降温结晶法制得FeCl3·6H2O,而不用直接蒸干的方法来
制得晶体的理由 。
21.(8分)有A、B、C、D、E、F、G、W八种气体,进行如下实验:
(1)分别将八种气体通入水中发现E、F难溶于水,其它气体可溶,其中A、D极易溶于水,W溶于水时有F气体生成
(2)A经催化氧化得F,C在空气中充分燃烧可得G
(3)C、D遇酸化的硝酸银分别有黑色沉淀和白色沉淀生成
(4)B与E化合得D,D与A相遇有大量白烟生成;
则:
A ,B ,C ,D ,E ,F ,G ,W ;
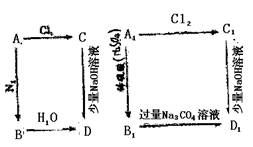 22.(8分)A和A1是同一周期的元素,在A和A1的如下图各步反应中,最后生成的D和D1均有白色沉淀。试推断:A、B、C、D;A1、B1、C1、D1,写出它们的化学式。
22.(8分)A和A1是同一周期的元素,在A和A1的如下图各步反应中,最后生成的D和D1均有白色沉淀。试推断:A、B、C、D;A1、B1、C1、D1,写出它们的化学式。
A B
C D
A1 B1
C1 D1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com