
题目列表(包括答案和解析)
7.下列情况可能引起水污染的是
①农业生产中农药、化肥使用不当 ②城市生活污水的任意排放 ③原子核反应的残留物随意排放 ④海上油轮石油泄漏⑤工业生产中废气、废液、废渣排放不当
A.①②③⑤ B.①③④⑤ C.①②③④ D.全部都是
解析:农药、化肥使用不当,城市生活污水的任意排放,海上油轮石油泄漏等皆可引起水污染。核反应的残留物会引起土壤和水污染,工业生产中的废气、废液、废渣的排放,可同时引起大气、水和土壤等污染。
答案:D
6.储存浓H2SO4的铁罐外口出现严重的腐蚀现象,这体现了浓硫酸的
A.吸水性和酸性 B.脱水性和吸水性
C.强氧化性和吸水性 D.不挥发性和酸性
解析:铁遇冷的浓硫酸会发生钝化,但浓硫酸具有较强的吸水性,吸水后变为稀硫酸,与活泼金属发生置换反应。
答案:A
5.向50 mL 18 mol·L-1的H2SO4溶液中加足量铜片并加热,充分反应后,被还原的H2SO4的物质的量为
A.小于0.45 mol B.等于0.45 mol
C.在0.45-0.90 mol之间 D.大于0.90 mol
解析:由反应式Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O,可知当H2SO4完全反应时,被还原的H2SO4的物质的量应为0.45 mol,但事实上H2SO4不可能完全反应(溶质减少,生成物中有水,H2SO4溶液变稀),故被还原的n(H2SO4)<0.45 mol。
CuSO4+SO2↑+2H2O,可知当H2SO4完全反应时,被还原的H2SO4的物质的量应为0.45 mol,但事实上H2SO4不可能完全反应(溶质减少,生成物中有水,H2SO4溶液变稀),故被还原的n(H2SO4)<0.45 mol。
答案:A
4.下列现象说明SO2具有氧化性的是
A.SO2通入品红溶液中使之褪色
B.SO2通入KMnO4酸性溶液中使之褪色
C.SO2通入溴水中使之褪色
D.SO2通入饱和H2S溶液中析出浅黄色沉淀
解析:SO2具有漂白性、氧化性、还原性。A中表现出漂白性,B、C中表现出还原性,只有D中(2H2S+SO2====3S↓+2H2O)表现出SO2的氧化性。
答案:D
3.下列有关硫的说法正确的是
A.硫可溶于水
B.硫易溶于二硫化碳
C.硫单质在与Cu、Fe、O2的反应中均作氧化剂
D.硫在自然界中仅以化合态存在
解析:硫不溶于水,所以A不正确。S与O2反应时生成SO2,硫作还原剂,所以C不正确。硫在自然界中主要以黄铁矿(FeS2)、黄铜矿(CuFeS2)等化合物形式存在,但在自然界中也存在单质硫,也叫自然硫,所以D不正确。硫易溶于二硫化碳中,所以B正确。
答案:B
2.下列气体中,若空气中含有微量时能使人产生爽快和振奋的感觉,但稍多时就会对人体,动、植物等造成危害的是
A.CO2 B.SO2 C.O3 D.O2
解析:空气中微量臭氧能刺激中枢神经,加速血液循环,令人产生爽快和振奋的感觉,但空气中臭氧的含量超过10-5%时,会对人,动、植物造成危害。而SO2只刺激呼吸系统,对呼吸系统造成危害。
答案:C
1.硒是氧族元素,下列关于硒及其化合物的叙述,不正确的是
A.硒化钠的熔点较高 B.硒难溶于水
C.硒化氢不能与二氧化硫反应 D.硒化氢有毒
解析:根据氧族元素递变规律,可知硒化氢和SO2能发生反应:2H2Se+SO2====2Se+S+2H2O。故C选项符合题意。由Na2O、Na2S熔点较高可推测Na2Se熔点也较高,由H2S有毒可推测H2Se也有毒,由S难溶于水可知单质硒亦难溶于水。故A、B、D三项不符合题意。
答案:C
15.(8分)
(1)3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O(2分)
(2)0.025mol(2分)
(3)0.005mol 0.005mol(4分)
(4)(0.015-x)mol (1分) (x-0.005)mol(1分) 0.005<X<0.015(2分)
13.(1)B
(2)①CaTiO3 ② 6
(3)①:H2TiO3
②:④⑤;
④: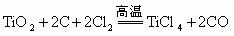 或⑤:
或⑤: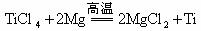
③:TiCl4+3H2O = H2TiO3+4HCl ; 共价
14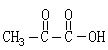


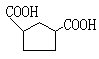 .(1)
.(1)
, 或
 (2)
(2)
12.(1) ,
, (2分/个,共4分)
(2分/个,共4分)
(2)① 3Fe2+ + NO3-+ 4H+ == 3Fe3+ + NO↑+ 2H2O(3分)
② 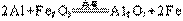 (3分)
(3分)
(3)0.2 mol/L(2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com