
题目列表(包括答案和解析)
18、下列有关阿伏加德罗常数的叙述正确的是( )
(A)标准状况下,以任意比混合的甲烷和丙烷混合气体22.4L所含分子数为NA个
(B)1mol冰醋酸中含有6.02×1023个CH3COO━
(C)电解饱和食盐水时,每得到1molNaOH,在阳极反应的离子就得到1mol电子
(D)标准状况下,1L辛烷完全燃烧后所生成气态产物的分子数为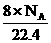
17、NA代表阿伏加德罗常数值,下列说法正确的是( )
(A)9g重水所含有的电子数为5NA
(B)1molMgCl2中含有离子数为NA
(C)7.1g氯气与足量NaOH溶液反应转移的电子数为0.2NA
(D)1molC10H22分子中共价键总数为31NA
16.(2006四川)室温下,在强酸性和强碱性溶液中都不能大量共存的离子组是
A.NH4+、Cu2+、Cl-、NO3- B.K+、Na+、SO32-、S2-
C.K+、Na+、AlO2-、SO42- D.Ba2+、Fe2+、NO3-、Br-
15、 下列反应的离子方程式书写正确的是
A.氯化铝溶液中加入过量氨水:Al3+
+ 4NH3•H2O
AlO2- + 4NH4+
+ 2H2O
B.澄清石灰水与少量苏打溶液混合:Ca2+ + OH- + HCO3-
CaCO3↓+ H2O
C.碳酸钙溶于醋酸:CaCO3
+ 2H+ Ca2+ + CO2↑ + H2O
D.氯化亚铁溶液中通入氯气:2Fe2+ + Cl2 2Fe3+ + 2Cl-
14、将纯水加热至较高温度,下列叙述正确的是
A.水的离子积变大、pH变小、呈酸性 B.水的离子积不变、pH不变、呈中性
C.水的离子积变小、pH变大、呈碱性 D.水的离子积变大、pH变小、呈中性
13、由硫酸钾、硫酸铝和硫酸组成的混合溶液,其pH=1,c(Al3+)=0.4 mol·L-1,c(SO42-)=0.8 mol·L-1,则c(K+)为
A.0.15 mol·L-1 B.0.2 mol·L-1 C.0.3 mol·L-1 D.0.4 mol·L-1
12、(2006全国)在0.1 mol·L-1 CH3COOH溶液中存在如下电离平衡:
CH3COOH  CH3COO-+H+ ,对于该平衡,下列叙述正确的是
CH3COO-+H+ ,对于该平衡,下列叙述正确的是
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.1mol·L-1HCl溶液,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向正反应方向移动
11.(2006重庆) 温度相同、浓度均为0.2 mol/L的 ①(NH4)2SO4、 ②NaNO3、 ③NH4HSO4、 ④NH4NO3、⑤ 、⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是
、⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是
A.③①④②⑥⑤ B.①③⑥④②⑤
C.③②①⑥④⑤ D.⑤⑥②④①③
10、羟胺(NH2OH)是一种还原剂,能将某些氧化剂还原。现用25.00mL0.049mol/L的羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+恰好与24.65mL 0.020mol/L的KMnO4酸性溶液完全作用(已知:FeSO4+ KMnO4+ H2SO4= Fe2(SO4)3+ K2SO4+ MnSO4+ H2O(未配平)),则在上述反应中,羟胺的氧化产物是( )
(A)N2 (B)N2O (C)NO (D)NO2
9、已知 I-、Fe2+、SO 2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为 Cl-< Fe 2+< H2O 2 < I-< SO 2,则下列反应不能发生的是( )
(A)2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ (B)I2+SO2+2H2O=H2SO4+2HI
(C)H2O2+H2SO4=SO2+O2+2H2O (D)2Fe2++I2=2Fe3++2I-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com