
题目列表(包括答案和解析)
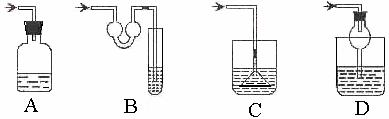
15、以下各种尾气吸收装置中,适合于吸收易溶性气体,而且能防止倒吸的是( )
14、常温下,0.1mol/LHX的pH=2,0.1mol/LCH3COOH pH约为2.9,下列说法正确的是
A.HX是一种强酸
B.将0.1mol的HCl与0.1mol的HX溶于水配成1L溶液,所得溶液的C(H+)=0.11mol/L
C.等物质的量浓度等体积的HX与NaX两溶液混合,溶液中离子浓度大小关系为:
c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-)
D.在同体积的0.1mol/L HX和0.1mol/L CH3COOH溶液中,分别加入0.1mol/L的NaOH溶液,欲使两者pH均等于7,则消耗氢氧化钠溶液的体积前者大于后者
13、阿伏加德罗常数约为6.02×1023mol-1。下列叙述中正确的是
A.标准状况下,2.24L苯中约含有3.612×1023个碳原子
B.常温常压下,氧气和臭氧的混合物16g中约含有6.02×1023个氧原子
C.25℃时,1L pH=13的氢氧化钠溶液中约含有6.02×1023个氢氧根离子
D.0.5molCH4中约含有3.01×1023个电子
12、下列反应的离子方程式书写正确的是
A.除去KNO3溶液中的Fe3+: Fe3++3H2O Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
B.硝酸铝溶液中加过量氢氧化钠溶液:Al3++3OH-=Al(OH)3↓
C.硫酸铜溶液中加入氢氧化钡溶液:Ba2++SO42-=BaSO4↓
D.硫酸亚铁溶液中加入过氧化氢溶液:2Fe2++H2O2+2H+=2Fe3++2H2O
11、将0.1mol铜与40mL10mol•L-1HNO3充分反应后,溶液中含amolH+,由此可知
A.生成的气体在标准状况下的体积为4.48L
B.生成的气体在标准状况下的体积为1.49L
C.被还原的硝酸的物质的量为(0.2-a)mol
D.反应后溶液中所含的NO3-的物质的量为0.2mol
10、 天然维生素P(结构如右图)存在于槐树花蕾中,它是一种营养增补剂。下列关于维生素P的叙述正确的是
天然维生素P(结构如右图)存在于槐树花蕾中,它是一种营养增补剂。下列关于维生素P的叙述正确的是
A.可以和溴水发生取代反应
B.属于不饱和酯类物质
C.分子中有三个苯环
D.1mol维生素P最多可以和7molH2反应
9、水蒸气中常含有部分(H2O)2,要确定(H2O)2的存在,可采用的方法是( )
A、1L水蒸气冷凝后与足量金属钠反应,测产生氢气的体积
B、1L水蒸气通过浓硫酸后,测浓硫酸增重的质量
C、该水蒸气冷凝后,测水的pH
D、该水蒸气冷凝后,测氢氧原子比
8、下列说法正确的是
A.分子晶体的熔点一定比金属的熔点低 B.在共价化合物中,各原子都能形成8电子结构
C.稀有气体的原子能形成分子晶体 D.离子化合物中一定含有金属元素
7、 浓硫酸和2mol/L的稀硫酸,在实验室中敞口放置。它们的质量和放置天数的关系如右图,分析a、b曲线变化的原因是( )
浓硫酸和2mol/L的稀硫酸,在实验室中敞口放置。它们的质量和放置天数的关系如右图,分析a、b曲线变化的原因是( )
A、a升华、b冷凝
B、a挥发、b吸水
C、a蒸发、b潮解
D、a冷凝、b吸水
6、下列说法正确的是(NA表示阿伏加德罗常数)
A.SiO2晶体中,有NA个Si就有2NA个Si-O键
B.P4分子中P和P-P键的比为2:3
C.常温常压下,1mol碳烯(:CH2)所含电子数为10NA
D.在10.6gNa2CO3固体中CO32-数目不到0.1NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com