
题目列表(包括答案和解析)
23.(10分)我国首创的铝、空气、海水电池为能源的新型海水标志灯已研制成功。这种灯以海水为电解质,靠空气中的氧使铝不断氧化而产生电流。
(1)上述新型电池_________为负极,正极的电极反应式为_____________________
(2)自然界存在的铝矿物主要有铝土矿,它是含有少量氧化铁和石英等杂质的氧化铝,工业上制备单质铝需要纯净的氧化铝,试写出以铝土矿、海水、贝壳(主要成分为碳酸钙)为原料提纯氧化铝的化学方程式。要求只写含有铝的化合物参加的化学反应方程式,是离子反应的要求写离子方程式。____________________________________ ______
22.(4分)铜是生命必需的元素,也人类最早使用的金属之一,铜的生产和使用对国计民生各个方面产生了深远的影响。在化学反应中,铜元素可表现为0、+1、+2价。
(1)在西汉古籍中曾有记载:曾青得铁则化为铜[即:曾青(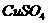 )跟铁反应就生成铜]。试写出该反应的化学方程式:_____________________________。
)跟铁反应就生成铜]。试写出该反应的化学方程式:_____________________________。
(2)铜器表面有时会生成铜绿[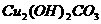 ],这层铜绿可用化学方法除去。试写出去铜绿而不损伤器物的反应的化学方程式:_________________________。
],这层铜绿可用化学方法除去。试写出去铜绿而不损伤器物的反应的化学方程式:_________________________。
21. (5分)在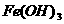 胶体溶液中,逐滴加入HI溶液,会发生一系列变化,请简述原因。
胶体溶液中,逐滴加入HI溶液,会发生一系列变化,请简述原因。
(1)开始出现红褐色沉淀,原因是_____________________________。
(2)随后沉淀溶解,溶液显黄色,原因是__________________________________,有关离子方程式为___________________________________.
(3)最后溶液颜色加深,原因是_________________________________________,有关离子方程式为___________________________________。
20、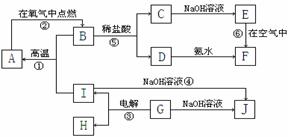 (10分)A-I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。请填写下列空白:
(10分)A-I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置___________________。
(2)写出C、G物质的化学式。C____________________ G______________________
(3)写出①、④、⑥反应的化学方程式。 反应①:___________________________________________________________ 反应⑥:___________________________________________________________
(4)从能量变化的角度看,①②③反应中属于△H<0的反应是___________。(填序号)
19.(10分)欲在13-2室温和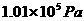 条件下测定镁的相对原子质量。请利用图13-2给定的仪器(盛放镁条的隔板有小孔)组成一套实验装置(每仪器只允许用一次)。
条件下测定镁的相对原子质量。请利用图13-2给定的仪器(盛放镁条的隔板有小孔)组成一套实验装置(每仪器只允许用一次)。
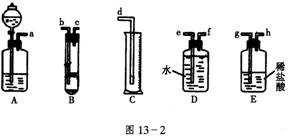 请回答下列问题:
请回答下列问题:
(1)假设气流方向为左→右,则各仪器的接口连接的先后顺序为(用小写字母填写)_________________________________。
(2)连接好仪器后,要进行的操作有以下几步:①待仪器B中的物质恢复至室温时,测量量筒C中水的体积(若假定将测定的体积换算成标准状况下V mL);②擦掉镁条表面的氧化膜,将其置于天平上称量(假定其质量为m并将其投入试管B中);③检查各装置的气密性;④旋开仪器A上分液漏斗活塞,当镁条完全溶解时再关闭活塞。上述几步操作的先后顺序是________________。
(3)根据实验数据可算出镁的相对原子质量,其数学表达式为________________________。
(4)若未将试管B冷却至室温就测量量筒C中水的体积,这将会使所测镁的相对原子质量数据(填“偏高”、“偏低”、“无影响”)_______________。
(5)若未擦净镁条表面氧化膜就进行实验,这将会使所测镁的相对原子质量数据(填“偏高”、“偏低”、“无影响”__________________。
18、向K2SO4 和FeCl3 的混合溶液中滴入Ba(OH)2溶液,当SO42-离子完全沉淀时,Fe3+离子也同时被完全沉淀,则原混合溶液中K2SO4 和FeCl3 的物质的量浓度之比为( )
A、3:1 B、3:2 C、2:1 D、2:3
第Ⅱ卷 (非选择题材 共46分)班级 分数
17.金属A和非金属B可以直接化合生成化合物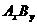 。甲、乙两同学分别做A和B化合的实验,每人所用A和B的质量不相同,但总质量12g,甲、乙所用A、B质量和得到的化合物
。甲、乙两同学分别做A和B化合的实验,每人所用A和B的质量不相同,但总质量12g,甲、乙所用A、B质量和得到的化合物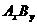 的质量如下:则A、B所发生的反应为
的质量如下:则A、B所发生的反应为
A.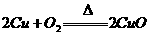 B.
B.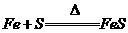 C.
C.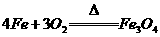
D.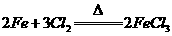
16. 把一块Al、Fe合金放入足量盐酸中,通入足量的Cl2 ,再加过量NaOH 溶液、过滤,把滤渣充分灼烧,得到固体残留物恰好与原合金质量相等,则合金中Fe、Al质量比为( )
A、1:1 B、3:1 C、1:4 D、7:3
|
|
A |
B |
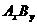 |
|
甲 |
8g |
4g |
11g |
|
乙 |
7g |
5g |
11g |
15.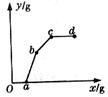 图13-1中y轴表示沉淀质量,x轴表示向某溶液中滴加的试济的质量。该图能表示下列过程中的(
)
图13-1中y轴表示沉淀质量,x轴表示向某溶液中滴加的试济的质量。该图能表示下列过程中的(
)
A.向用盐酸酸化的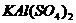 溶液中滴加
溶液中滴加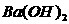 溶液
溶液
B.向磷酸溶液中滴加澄清石灰水
C.向硫酸溶液中滴加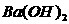 溶液
溶液
D.向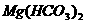 溶液中滴加NaOH溶液并煮沸
溶液中滴加NaOH溶液并煮沸
14.2004年5月,保利集团在香港拍卖会上花费3000多万港币购回在火烧圆明园时流失的国宝:铜铸的牛首、猴首和虎首。普通铜器时间稍久容易出现铜绿,其主要成份是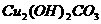 。这三件1760年铜铸的国宝在240年后看上去仍然熠熠生辉不生锈,下列对其原因的分析,最可能的是( )
。这三件1760年铜铸的国宝在240年后看上去仍然熠熠生辉不生锈,下列对其原因的分析,最可能的是( )
A.它们的表面都电镀上一层耐腐蚀的黄金 B环境污染日趋严重,它们表面的铜绿被酸雨溶解
C.铜的金属活动性比氢小,因此不易被氧化D.它们是含一定比例金、银、锡、锌的铜合金
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com