
题目列表(包括答案和解析)
24、(4分)设X、Y、Z代表三种元素。已知:
① 和
和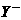 两种离子具有相同的电子层结构;
两种离子具有相同的电子层结构;
②Z元素原子核内质子数比Y元素原子核内质子数少9个;
③Y和Z两种元素可以形成4核42个电子的负一价阴离子。
据此,请填空:
(1)Y元素是 ,Z元素是 。
(2)由X、Y、Z三种元素所形成的含68个电子的盐类化合物的化学式是 。
23、(8分)X、Y、Z为短周期元素的单质,U、V为它们的化合物,这些物质之间的关系如右图所示,其中反应条件和某些产物已经略去:
(1)如果X、Y的组成元素是同主族的,写出反应I的化学反应方程式:
 ①若已知V是水:
。
①若已知V是水:
。
②若已知U、V均为氧化物: 。
(2)如果X、Y的组成元素不同主族时,按下列要求回答问题。
①若X组成元素是地壳中含量最多的金属元素时,则X、Y、Z的化学式是:X为 ;Y为 ;Z为 。
②若Y组成元素在自然界中形成的化合物种类最多时,则V、U的化学式是:V为 ;U为 。
③若Z是通常情况下密度最小的物质,则反应I的化学反应方程式: 。
22、 (6分)已知A、B、C、D四种不同粒子。他们之间存在如下关系:
(6分)已知A、B、C、D四种不同粒子。他们之间存在如下关系:
(1)如果A、B、C、D均是10电子的粒子,则A的结构式为
;D的电子式为 。
(2)如果A为一种金属阳离子,且A、B、D均为10电子粒子,C为30电子粒子。试写出:
A与B在溶液中反应生成C和D的离子方程式 。
C与H+反应生成A的离子方程式 。
21、(6分)下表是元素周期表的一部分:
 |
I A |
ⅡA |
ⅢA |
ⅣA |
VA |
ⅥA |
ⅦA |
|
1 |
① |
|
|||||
|
2 |
② |
③ |
④ |
|
⑤ |
⑥ |
|
|
3 |
|
⑦ |
⑧ |
|
|
⑨ |
⑩ |
(1)表中元素⑩的氢化物的化学式为 ,此氢化物的还原性比元素⑨的氢化物的还原性 (填“强”或“弱”)。
(2)某元素的核外K层电子数比L层电子数少3,则该元素的元素符号是 ,其单质的电子式为 。
(3)俗称为“矾”的一类化合物通常含有的共同元素是 。
(4)已知某些不同族元素的性质也有一定的相似性,如元素③与⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与 溶液反应的化学方程式
。
溶液反应的化学方程式
。
又如表中与元素⑦的性质相似的不同族的元素是 (填元素符号)。
20、(6分)假定元素同期表是有限的,根据已知的元素周期表的某些事实和理论可归纳出一些假说。
(1)根据每个周期最后一种金属元素出现的族序数,预测周期表中原子序数最大的金属元素将在 周期 族(注意:把零族看作ⅦA族);周期表在填满 周期后将结束。
(2)根据周期表中每个周期非金属元素的种数(把稀有气体看作非金属)预测周期表中应该有 种非金属元素,还有 种未发现,未发现的非金属处在 周期 族。
19、(6分)不同元素的气态原子失去最外层一个电子所需要的能量(设其为E)如下图所示。试根据元素在周期表中的位置,分析图中曲线的变化特点,并回答下列问题。
(1)同主族内不同元素的E值变化的特点是: ;各主族中E值的这种变化特点体现了元素性质的 变化规律。
(2)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常现象。试预测下列关系中正确的是 (填写编号)。
①E(砷)>E(硒) ②E(砷)<E(硒) ③E(溴)>E(硒) ④E(溴)<E(硒)
(3)估计1 气态
气态 原子失去最外层一个电子所需能量E值的范围:
原子失去最外层一个电子所需能量E值的范围:
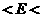 。
。
(4)10号元素E值较大的原因是 。
18、一些科学家预言,存在稳定的超重元素,如N=184的原子,它位于元素周期表第七周期,第ⅠNA族,由此,下列说法正确的是 ( )
A.第七周期有50种元素 B.该原子的质子数是184
C.该元素的相对原子质量是298 D.该原子核外有114个电子
第Ⅱ卷(非选择题,共51分)
17、A、B、C、D均为短周期的4种元素,当A、B两种元素的两个原子分别得到两个电子形成稳定结构时A放出的能量大于B放出的能量,当C、D两元素的原子分别失去1个电子形成稳定结构时D吸收的能量大于C吸收的能量。若A、B、C、D4种元素间分别形成化合物时属于离子化合物可能性最大的是 ( )
A.C2A B.C2B C.D2A D.D2B
16、两种短周期元素形成的化合物中,原子个数比为1:2或2:1,若两种元素的原子序数分别为p和q,则下列关系正确的是 ( )
① ②
②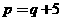 ③
③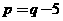 ④
④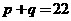
A.①④ B.①③④ C.①②③④ D.①②④
15、A、B为短周期元素,两者能形成型离子化合物,A离子比B离子少一个电子层,已知B的原子序数为x,则A的原子序数为 ( )
A. 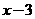 B.
B.  C.
C. 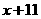 D.
D. 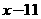
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com