
题目列表(包括答案和解析)
9、高温下硫酸亚铁发生如下反应:2FeSO4 Fe2O3+SO2↑+SO3↑,若将生成的气体通入氯化钡溶液中,得到的沉淀物是( )
Fe2O3+SO2↑+SO3↑,若将生成的气体通入氯化钡溶液中,得到的沉淀物是( )
A BaSO3和BaSO4 B BaS C BaSO3 D BaSO4
8、在强酸溶液中,下列各组离子能够大量共存的是 ( )
A.Mg2+、Ca2+、HCO3-、CI- B.Na+、AIO2-、Cl-、SO42-
C.K+、Fe2+、SO42-、Br- D.Fe2+、Ca2+、CI-、NO3-
7、在氧气中灼烧0.44 g硫和铁组成的化合物,使其中的硫全部转变为二氧化硫,把这些二氧化硫全部氧化并转变为硫酸.这些硫酸可以用20 mL 0.5 mol/L的氢氧化钠溶液完全中和.则原化合物中硫的质量分数为( )
A.18% B.46 % C.53% D.36%
6.含FeS2 A%的黄铁矿W t,在接触法制H2SO4的过程中,损失硫C%,可制得浓度为B%的硫酸为( )
A.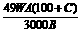 t B.
t B.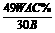 t C.
t C.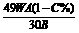 t D.
t D.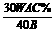 t
t
5、现有1 L含SO3为30%的发烟硫酸(密度为1.95 g·cm-3),要把它稀释成浓度为95%的浓硫酸,要加水约为( )
A.120 mL B.180 mL C.240 mL D.300 mL
4、对于反应4FeS2 + 11O2 = 2Fe2O3 +8SO2 ,下列叙述正确的是( )
A、铁和硫两种元素被还原
B、转移的电子数是40
C、Fe2O3和SO2都既是氧化产物,又是还原产物
D、由于O2过量,SO2部分被氧化为SO3
3、下列反应中,调节反应物用量或浓度不会改变反应产物的是(1998年上海高考题)
A.硫化氢在氧气中燃烧 B.铁在硫蒸气中燃烧
C.二氧化硫通入石灰水 D.硫酸中加入锌粉
2、在硫酸工业生产中,为了有利于SO2的转化,且能充分利用热能,采用了中间有热交换器的接触室(见右图),按此密闭体系中气体的流向,则从A处流出的气体为( )
A.SO2 B.SO3、O2
C.SO2、O2 D.SO2、SO3
1、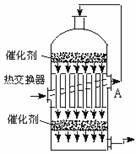 导致下列现象的主要原因与排放SO2有关的是(2000年全国高考题)
A.酸雨 B.光化学烟雾 C.臭氧空洞 D.温室效应
导致下列现象的主要原因与排放SO2有关的是(2000年全国高考题)
A.酸雨 B.光化学烟雾 C.臭氧空洞 D.温室效应
18. A、B、C、D是四种短周期元素,已知A、C同主族,B、D同周期,A的气态氢化物比C的气态氢化物稳定;B的阳离子比D的阳离子氧化性强,若B的阳离子比C的阴离子少一个电子层,下列比较不正确的是( )
A.原子序数:A>B>C>D B.原子半径:D>B>C>A
C.单质熔点:D>B,C>A D.简单离子半径:C>A>D>B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com