
题目列表(包括答案和解析)
4.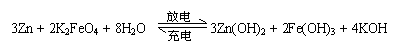 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为(江苏)
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为(江苏)
下列叙述不正确的是( )
A.放电时负极反应为:Zn-2e- +2OH-= Zn(OH)2
B.充电时阳极反应为:Fe(OH)3 -3e- + 5 OH- = FeO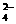 + 4H2O
+ 4H2O
 C.放电时每转移3 mol电子,正极有1mol K2FeO4被氧化
C.放电时每转移3 mol电子,正极有1mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
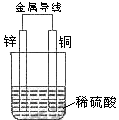
3.金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是( )(天津)(已知:氧化性Fe2+<Ni2+<Cu2+)
A.阳极发生还原反应,其电极反应式:Ni2+ + 2e- == Ni
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.电解后,溶液中存在的金属阳离子只有Fe2+ 和Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt
2.关于电解NaCl水溶液,下列叙述正确的是( )(全国卷I)
A.电解时在阳极得到氯气,在阴极得到金属钠
B.若在阳极附近的溶液中滴入KI试液,溶液呈棕色
C.若在阴极附近的溶液中滴入酚酞试液,溶液呈无色
D.电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性
1.可以将反应Zn+Br2=ZnBr2设计成蓄电池,下列4个电极反应
①Br2+2e=2Br- ②2Br--2e=Br2 ③Zn-2e=Zn2+ ④Zn2++2e=Zn
其中表示充电式的阳极反应和放电时的负极反应的分别是( )
A.②和③ B.②和① C.③和① D.④和①
25、(8分)某化工厂以硫磺为原料生产硫酸,设空气中O2的体积含量为21%,不考虑各阶段物料损失,完成下列各题:
(1)若该厂生产98%的硫酸10t,需要硫磺的质量是__________________t,需要消耗标况下的空气的体积______________________m3.
(2)若该厂每天生产98%的硫酸a t,生产过程中为了使硫充分燃烧,且下一步催化氧化时不再补充空气,要求硫燃烧后的混合气体中O2的体积分数为b%,该厂每天消耗标况下的空气的体积为___________________________m3,为满足题设要求,b%的下限等于___________________。
24、(10分)某化学兴趣小组选用下列实验装置图,测定工业原料气(含SO2、N2、O2)中SO2的含量。
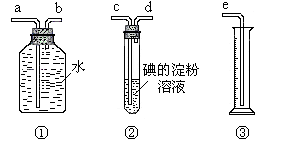
(1)若原料气从左到右流向时,上述装置组装连接的顺序是:原料气→______________(填a、b、c、d、e等)
(2)装置②中发生反应的离子方程式为_______________________;当装置②中出现____________________现象时,立即停止通气.
(3)你认为下列试剂中,可以用来代替试管中的碘的淀粉溶液的是____________.
A.酸性KMnO4 B.NaOH溶液 C.溴水 D.氨水
(4)若碘溶液的浓度为0.05mol/L,体积为20mL,收集到的N2与O2的体积为297.6mL(已折合为标况体积),SO2的体积分数为________________
23、(7分)下图每一个方框中的字母代表一种反应物或生成物,它们都是中学化学中常见的物质,其中A、C都是由两种元素组成的固态化合物,常温下甲是短周期元素的气体单质,E是过渡元素的单质。

(1)若A是黄色固体,反应①用于工业生产,则A的化学式为________________.此时反应②的化学方程式为_______________________________________.
(2)若A、C都是黑色固体,A经反应①生成C时,固体质量不变,则A的化学式为____________.
(3)反应③在工业生产中的条件是_________________________________________.
22、(7分)A、B两种盐的式量均为120,A、B的焰色反应分别为黄色和紫色,A、B的溶液混合产生一种有刺激性气味气体C,向A、B中加入Ba(OH)2溶液分别产生白色沉淀D、E,E能溶于稀盐酸中,也产生气体C。
(1) 写出A、B、C、D、E的化学式:A______B______D______。
(2)写出下列有关离子方程式:A+B___________________________________
B+Ba(OH)2____________________________________________。
21、(8分)X、Y、Z是短周期元素的3种常见氧化物,X跟水反应后可生成一种具有还原性的不稳定的二元酸,该酸的化学式是__________________,Y和X 的组成元素相同,Y的化学式是____________________,1mol Z在加热时跟水反应的产物需要用6mol的氢氧化钠才能完全中和。在一定条件下,Y可以跟非金属单质A反应生成X和Z,单质A是________,该反应方程式为____________________.
20、 某化工厂工业废水中含H2SO4的质量分数为2%,采用边排放边中和的方法将它处理至基本呈中性,处理方法如下图所示,若处理后废水的PH=7,则2%的NaOH溶液的流量为( )
某化工厂工业废水中含H2SO4的质量分数为2%,采用边排放边中和的方法将它处理至基本呈中性,处理方法如下图所示,若处理后废水的PH=7,则2%的NaOH溶液的流量为( )
A、0.00816m3/s B.0.01m3/s
C.0.01632m3/s D.0.02m3/s
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com