
题目列表(包括答案和解析)
14.25-12) x=4.5
③ O2过量 4Cu + O2 → 2Cu2O
104.(03上海,33)黄铜矿(主要成分CuFeS2)是提取铜的主要原料
(1)取12.5 g黄铜矿样品,经测定含3.60 g硫(杂质不含硫),矿样中CuFeS2含量为
(2)已知:2CuFeS2+4O2  Cu2S+3SO2+2FeO(炉渣)
Cu2S+3SO2+2FeO(炉渣)
产物Cu2S在1200℃高温下继续反应:
2Cu2S + 3 O2 → 2Cu2O + 2 SO2
2 Cu2O + Cu2S → 6Cu + SO2
假定各步反应都完全,完成下列计算:
① 由6 mol CuFeS2生成6 mol Cu,求消耗O2的物质的量
② 6 mol CuFeS2和14.25 mol O2反应,理论上可得到多少摩尔铜?
③ 6 mol CuFeS2和15.75 mol O2反应,理论上可得到多少摩尔铜?
答案:(1)82.8% (2)① CuFeS2  Cu+FeO+2SO2
Cu+FeO+2SO2
n(O2)=(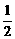 +2)×6 mol=15 mol
+2)×6 mol=15 mol
② O2不足量 2CuFeS2+4O2  Cu2S+3SO2+2FeO
Cu2S+3SO2+2FeO
6 mol 12 3
Cu2S + O2 ® 2Cu+SO2
103.(03广东,25)取一定量的Na2CO3、NaHCO3和Na2SO4混合物与250mL 1.00mol·L-1过量盐酸反应,生成2.016L CO2(标准状况),然后加入500mL 0.100mol·L-1Ba(OH)2溶液,得到沉淀的质量为2.33g,溶液中过量的碱用10.0mL 1.00ml·L-1盐酸恰好完全中和。计算混合物中各物质的质量。
答案:m(Na2CO3)=7.42g m(NaHCO3)=1.68g
0.915 g/cm3的氨水。试计算1体积水吸收多少体积的氨气可制得上述氨水。
(本题中氨的式量以 17.0计,水的密度以1.00 g/cm3计)
答案:1体积水吸收378体积NH3气(标准状况)
102.(01全国,25)标准状况下,用一定量的水吸收氨气后制得浓度为12.0 mol/L、密度为
101.(01全国,21)在120 ℃时分别进行如下四个反应:
A.2H2S+O2 ==2H2O+2S B.2H2S+3O2 ==2H2O+2SO2
C.C2H4+3O2==2H2O+2CO2 D.C4H8+6O2==4H2O+4CO2
(1)若反应在容积固定的容器内进行,反应前后气体密度(d)和气体总压强(p)分别符合关系式d前=d后和 p前> p后的是____________;符合关系式d前=d后和 p前= p后的是__________________(请填写反应的代号)。
(2)若反应在压强恒定容积可变的容器内进行,反应前后气体密度(d)和气体体积(V)分别符合关系式d前>d后和 V前<V后的是____________;符合d前>d后和 V前>V后的是_________________(请填写反应的代号)。
答案:(1)B;C (2)D;A
100.(01全国,20)某学生利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量。实验步骤如下:
①把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量,质量为a g。
②装好实验装置。
③检查装置气密性。
④加热,开始反应,直到产生一定量的气体。
⑤停止加热(如图,导管出口高于液面)。
⑥测量收集到气体的体积。
⑦准确称量试管和残留物的质量为b g。
⑧测量实验室的温度。
⑨把残留物倒入指定的容器中,洗净仪器,放回原处,把实验桌面收拾干净。
⑩处理实验数据,求出氧气的摩尔质量。

回答下列问题:
(1)如何检查装置的气密性?____________________________________________。
(2)以下是测量收集到气体体积必须包括的几个步骤;①调整量筒内外液面高度使之相同;②使试管和量筒内的气体都冷却至室温;③读取量筒内气体的体积。这三步操作的正确顺序是:__________________________________(请填写步骤代号)
(3)测量收集到气体体积时,如何使量筒内外液面的高度相同?
____________________________________________________________。
(4)如果实验中得到的氧气体积是c L(25 ℃、1.01×l05 Pa),水蒸气的影响忽略不计,氧气的摩尔质量的计算式为(含a、b、c,不必化简):
M(O2)= __________________________________________。
答案:(1)将导管的出口浸入水槽的水中,手握住试管,有气泡从导管口逸出,放开手后,有少量水进入导管,表明装置不漏气。
(2)②①③
(3)慢慢将量筒下移 (4)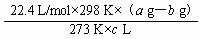
99.(01广东,23)已知脊椎动物的骨骼中含有磷。以下是测定动物骨灰中磷元素含量的实验方法。称取某动物骨灰样品0.103 g,用硝酸处理,使磷转化成磷酸根。再加入某试剂,使磷酸根又转化成沉淀。沉淀经灼烧后得到组成为P2Mo24O77的固体(其式量以3.60×103计)0.504 g。
试由上述数据计算该骨灰样品中磷的质量分数。(磷的相对原子质量以31.0 计。)
答案:n(P2Mo24O77)=(0.504 g / 3.60×10.3 g·mol-1)
其中P的质量为:(0.504 g × 2 × 31.0 g·mol-1)/(3.60×10.3 g·mol-1)
P的质量分数:(0.504 g × 2 × 31.0 g·mol-1)/(3.60×103 g·mol-1 × 0.103 g)=0.0843 (或8.43%)
98.(00全国,29)将某温度下的KNO3溶液200g蒸发掉10g水,恢复到原温度,或向其中加入10gKNO3固体,均可使溶液达到饱和。试计算:
(1)该温度下KNO3的溶解度。
(2)原未饱和溶液中溶质的质量分数。
答案:(1)该温度下KNO3的溶解度为100g (3分)
(2)原来饱和溶液中溶质的质量分数为47.5%
蒸发掉10gH2O得到190g饱和溶液,根据溶解度其溶质为95g。故原来饱和溶液中溶质的质量分数为
(或加10gKNO3得到210g饱和溶液,其溶质为105g。故原来饱和溶液中溶质为95g,质量分数为 )
)
97.(99上海,33)自然界存在的碳酸盐类铜矿(如孔雀石、石青等)的化学组成为:aCuCO3·bCu(OH)2 (a,B为正整数,且a≤2b≤2为正整数,且(1)将孔雀石、石青矿样分别加盐酸至完全溶解,耗用HCl物质的量与产生CO2物质的量之比:孔雀石为4:1;石青为3:1。它们的化学组成为:孔雀石:石青:(2)今有一份碳酸盐类铜矿样品,将其等分为A、B两份。然后,加盐酸使A样品完全溶解,产生CO233.6L(标准状况);加热B样品使其完全分解,得到20gCuO。试计算并确定该矿石的化学组成。(3)某碳酸盐类铜矿样加酸完全溶解后,产生CO26.72L(标准状况),这份矿样中CuO含量不低于 克(4)设某碳酸盐类铜矿样的质量为A克,所含CuO质量为G克。加酸完全溶解后,产生的CO2体积(标准状况)为V升,则含铜矿样的A、V、G之间的关系式为:A=
答案:(1)孔雀石 CuCO3·Cu(OH)2 石青 2 CuCO3·Cu(OH)2 (2)组成为: CuCO3·Cu(OH)2与2 CuCO3·Cu(OH)2混合物 (3)36克 (4)A=124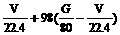
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com