
题目列表(包括答案和解析)
8.2005年4月22日是第36个“世界地球日”,我国国土资源部确定今年“世界地球日”的主题为“善待地球-科学发展,构建和谐”。你认为下列行为中不符合这一主题的是
A.开发太阳能、水能、风能、可燃冰等新能源、减少使用煤、石油等化石燃料
B.控制含磷剂的生产和使用,防止水体富营养化,保护水资源
C.研究采煤、采油新技术,尽量提高产量以满足工业生产的快速发展
D.实现资源的“3R”利用观,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、资源的循环再生(Recycle)
7.下图是一种正在投入生产的大型蓄电系统。左右两侧为电解质储罐,中央为电池,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过;放电前,被膜隔开的电解质为Na2S2(右罐)和NaBr3(左罐),放电后,分别变为Na2S4和NaBr。下列说法正确的是
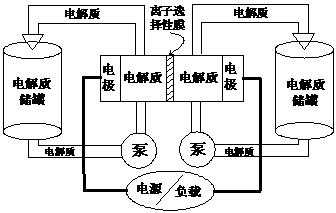
A.电池充电时,阳极电极反应式为:3Br-2e-=Br3-
B.电池放电时,负极电极反应式为:2S22-+2e-==S42-
C.电池放电时,电池的总反应方程式为:Na2S4+3NaBr=2Na2S2+NaBr3
D.在放电过程中Na+通过膜的流向为从左到右
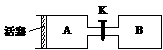
6.右图A、B是等体积容器,K是开关,活塞可以左右移动。在一定温度下,关闭K,向A中通入一定量的NO2。发生:2NO2(g)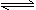 N2O4(g);△H<0。则以下说法正确的是
N2O4(g);△H<0。则以下说法正确的是
A.保持活塞位置不变,打开K,体系中气体颜色先变浅、然后略加深
B.打开K一会,再关闭它,向右推动活塞时,最后A容器的气体颜色比B的浅
C.打开K一会,再关闭它,把A容器加热,活塞向右移动,A中气体颜色变浅
D.打开K一会,再关闭它,向B中通入氩气,B中气体颜色变浅
5.取0.2mol·L-1HX溶液与0.2mol·L-1NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH = 8,则下列说法(或关系式)不正确的是
A.混合溶液中由水电离出的c(OH¯)>0.2mol·L-1HX溶液中由水电离出的c(H+)
B.c(Na+) = c(X¯) + c(HX) = 0.2mol·L-1
C.c(Na+)-c(X¯) = 9.9×10-7mol·L-1
 D.c(OH¯)-c(HX) = c(H+) = 1×10-8mol·L-1
D.c(OH¯)-c(HX) = c(H+) = 1×10-8mol·L-1
4.2005年12月1日为世界第18个艾滋病日,截至2005年9月底,全国累计报告艾滋病病毒感染者超过13万。医学界通过放射性14C标记的C60,发现C60的羧酸衍生物在特定条件下可断裂DNA杀死细胞,抑制艾滋病。关于14C的下列说法中正确的是
A.14C原子与C60中普通碳原子的化学性质不同
B. 14C原子与14N原子所含中子数相同
C.与12C、13C是碳元素的三种同位素
D.是C60的同素异形体
3.设NA表示阿伏加得罗常数,下列叙述正确的是
A.标准状况下,11.2L氦气所含的原子数为NA
B.1.6gNH2-离子中所含的电子数为NA
C.常温常压下,44g二氧化碳分子中所形成的共用电子对数为2NA
D.NA个氮分子和NA个氢分子的体积比是1︰1
2.Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1︰16,则x值是
A.2 B.3 C.4 D.5
1.某溶液能使红色的石蕊试纸先变蓝色后褪色,则该溶液中可能大量共存的离子组是
A.K+、I-、AlO2-、HCO3-、MnO4- B.Na+、S2- 、NO3-、SO32-、SO42-
C.Fe2+、Al3+、NH4+、NO3-、F- D.K+、Na+、Cl-、ClO-、CO32-
31.钙是人体神经、肌肉、骨骼系统、细胞膜和毛细血管通透性的功能正常运作所必需的常量元素,维生素D参与钙和磷的代谢作用,促进其吸收并对骨质的形成和改善有重要的作用。某制药有限公司生产的“钙尔奇D600片剂”的部分文字说明如下:“本品每片含主要成分碳酸钙1.5 g (相当于钙元素600 mg),成人每天服用1片。”
(1) “1.5 g碳酸钙与600 mg的钙”的计量关系是如何得出来的,请列式并计算表示
(2) 该公司的另一种产品,其主要成分与“钙尔奇D600”相同,仅仅是碳酸钙的含量不同。为测定该片剂中碳酸钙含量,某学生进行了如下实验:取10片该片剂碾碎后放入足量的HCl中经充分反应(假设该片剂的其余部分不与HCl 反应)过滤,取滤液加(NH4)2C2O4,使Ca2+ 生成CaC2O4沉淀,沉淀过滤洗涤后溶解于强酸中,并稀释成1 L溶液,取其20.0 mL,然后用0.0500 mol/LKMnO4 溶液滴定,反应中用去12 .0 mL KMnO4溶液,发生的离子反应为:
2MnO4― +5H2C2O4 +6H+ 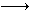 2Mn2+ +10CO2↑+8H2O
2Mn2+ +10CO2↑+8H2O
① 请通过计算回答该片剂中碳酸钙的含量。
② 参照上述关于“钙尔奇D600片剂”的文字说明,你认为该片剂的名称应该叫“钙尔奇D________ 片剂”。
30.向550 g密度为1.1 g/cm3的未知浓度的硫酸铜溶液中加入一定量的氢氧化钠溶液,经过滤、干燥得到19.6 g蓝色固体。在滤液中加入过量的铁粉,充分反应后,再加入足量的盐酸,最后得到6.4 g 固体,求原溶液的物质量浓度。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com