
题目列表(包括答案和解析)
3、某化工厂的废液经测定得知主要含有乙醇,其中还溶有苯酚(熔点:43℃)、乙酸和少量二氯甲烷。现欲从废液中回收它们,根据各物质的熔点和沸点,该工厂设计了以下回收的实验方案。
|
物质 |
乙醇 |
乙酸 |
二氯甲烷 |
苯酚 |
|
沸点/℃ |
78 |
117.9 |
40 |
181.7 |
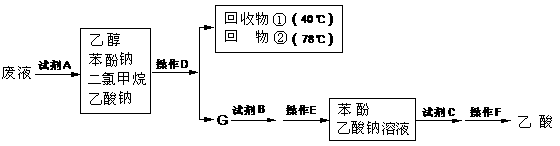
请回答:(1)写出试剂A、B、C的化学式:A ,B ,C ;
(2)写出操作D的名称:D ;
(3)写出回收物①、②和G的组成:① ,② ,G 。
2、(1)进行下列各项定量试验,由于某步操作不符合要求,可能会造成结果偏低的有 (在本题得分范围内选错倒扣分)。
(A)欲取2.0g食盐,用托盘天平(指针向上),称完读数时指针偏向右边。
(B)用容量瓶配制溶液,摇匀后,发现液面低于刻度线,于是准确地再滴加蒸馏水到刻度线摇匀。
(C)用量筒量液体,读数时俯视。
(D)酸式滴定管滴定后读数时俯视。
(E)测定晶体硫酸铜结晶水含量,加热坩埚蒸发水分,由于温度超过650℃部分晶体由蓝色变为黑灰色。
(F)测定硝酸钾溶解度,取10mL水于试管中,逐渐加入盐搅拌。测量温度时,试管里未见不溶晶体残存。
(2)、回答下面问题:
①分离沸点不同但又互溶的液体混合物,常用什么方法? 。
②在分液漏斗中用一种有机溶剂提取水溶液里的某物质时,静量分层后,如果不知道哪一层液体是“水层”,试设计一种简便的判断方法。 。
1、可用于分离或提纯物质的方法有: A.分馏B.盐析C.过滤D.重结晶E.升华F.渗析G.电解H.加热I.蒸馏。下列各组混合物的分离或提纯应选用哪一种方法最合适?
(1)除去Ca(OH)2溶液中悬浮的CaCO3微粒,用 。
(2)除去Fe(OH)3胶体中混有的Cl-,用 。
(3)除去乙醇中溶解的微量食盐,用 。
(4)分离石油中各种不同沸点范围的成分,用 。
(5)除去固体碘中混有的少量NaI,用 。
(6)除去CaO中的CaCO3,用 。
30.将30℃时物质A的溶液136g分成两等份,向其中一份加入10 gA,结果只溶解了2 g就不再溶解;将另一份溶液降温至0℃,析出A 5.5 g,此时溶液中A的质量分数为20%,已知A中不含结晶水,则A在30℃时的溶解度为
A.40g B.30g C.20g D.22g
29.中国学者许志福和美国科学家穆尔共同合成了世界上最大的碳氢分子,其中1个分子由1134个碳原子和1146个氢原子构成。关于此物质,下列说法错误的是
A.是烃类化合物 B.常温下呈固态
C.具有类似金刚石的硬度 D.易被氧化
28.一密闭容器中,aA(g)  bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
A.平衡向正反应方向移动了 B. 物质A的转化率减少了
C.物质B的质量分数增加了 D. a>b
27.已知强酸与强碱完全反应的中和热为57.3kJ/moL,且生成沉淀要放出热量,下列反应的|△H |值大于57.3kJ/moL的是
A.1/2H2SO4(aq)+1/2Ba(OH)2(aq)=1/2BaSO4(s)+H2O(l)
B.2KOH(aq)+H2SO4(aq)=K2SO4(aq)+2H2O(l)
C.CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l)
D.NH3·H2O(aq)+HCl(aq)=NH4Cl(aq)+H2O(l)
26.常温下,将pH=5的硫酸溶液稀释到原来的500倍,则溶液中[SO42-]与[H+]之比约为
A.1:1 B.1:2 C.1:10 D.10:1
25.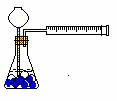 可用推拉注射器活塞的方法检查图中装置的气密性。当缓慢拉活塞时,如果装置气密性良好,可观察到:
可用推拉注射器活塞的方法检查图中装置的气密性。当缓慢拉活塞时,如果装置气密性良好,可观察到:
A.长颈漏斗下端口产生气泡
B.瓶中液面明显上升
C.长颈漏斗内有液面上升
D.注射器内有液体
24.把一小块镁、铝合金放入 6mol·L-1的NaOH溶液中,可以形成微型原电池。则该原电池负极上发生的电极反应为
A.Mg-2e-=Mg2+ B.Al+4OH--3e-=AlO2-+2H2O
C.4OH--4e-=2H2O+O2↑ D.2H2O+2e-=2OH-+H2 ↑
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com