
题目列表(包括答案和解析)
22.(8分)(1)已知下列反应在一定条件下可以发生:
H2O2+ 2Fe2++2H+=2Fe3++ 2H2O H2O2+2Fe3+=2Fe2++ O2↑+2H+
在以上反应中Fe2+实际上起着 作用,总反应式为
(2) I2与Fe2+一样发生上述类似反应,类比(1)在下面填入配平的合适的化学反应方程式:H2O2+I2=2HIO, ,总反应式为
(3)在硫酸和KI的混合溶液中加入足量的H2O2,放出大量的无色气体,溶液呈棕色,并可使淀粉变蓝色。有学生认为该反应的离子方程式为:H2O2+2I-= O2↑+2H++I2,这个方程式正确吗?若正确,理由是(若认为不正确,该步不必作答) 。
若不正确,原因是(若认为正确,该步不必作答) ,并写出正确的化学反应方程式为(若是离子反应,写出离子反应方程式,没有离子反应的,写出化学反应方程式)
21.(6分)在温度为373K时,把11.5g N2O4气体通入体积为500ml的真空密闭容器中立即出现红棕色,反应进行到2s时,NO2含量为0.01mol,进行到60s时,达到平衡,此时容器中混合气体的密度是氢气密度的28.75倍,则:
⑴开始时2s内以c(N2O4)的变化表示的反应速率是____________
⑵达到平衡时体系内的压强是开始的____________倍
20.(10分)二氯化硫(SCl2)熔点-78℃,沸点59℃。密度1.638。遇水易分解。二氯化硫与三氧化硫作用可生成重要化工试剂亚硫酰氯(SOCl2)。以下是由氯气与硫反应合成二氯化硫的实验装置。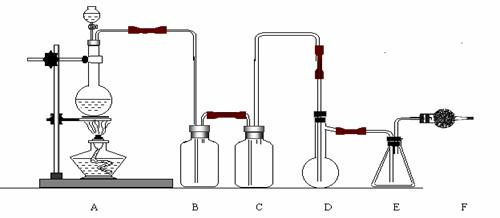
试回答下列问题:
(1)装置A中发生反应的化学方程式为: 。
(2)装置C盛放的药品是 。
(3)实验开始前先在D中放入一定量的硫粉,加热使硫熔化,然后转动和摇动烧瓶使硫附着在烧瓶内壁形成一薄层表面,这样做的目的是 。
(4)实验时,D装置需加热至50-59oC,最好采用何种方式 加热 。
(5)F装置中干燥管内所盛物质的作用是: 。
19、(I)__________________ (II)(1)______________
(2)证明KClO3中含有K、Cl、O三种元素的实验步骤及每一步的实验目的是
① ;
② ;
③ ;
④ 。
19.(12分)请按要求填空:
(Ⅰ)下列操作正确的是____________________(填数字编号)
①将未经湿润的pH试纸浸到某溶液中,过一会取出与标准比色卡比较,测得该溶液pH
②制备Fe(OH)2时,将盛NaOH(aq)的滴管伸入到试管内FeSO4(aq)的液面下
③焰色反应操作是:将铂丝放在稀盐酸中洗涤,然后蘸取待检物置于酒精灯或煤气灯的火焰上灼烧,观察火焰的颜色
④中和滴定中,锥形瓶用蒸馏水洗净后直接往其中注入一定量的待测溶液
⑤各放一张质量相同的滤纸于天平的两托盘上,将NaOH固体放在左盘纸上称量
⑥配置0.1mol·L-1的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释
⑦用渗析法除去淀粉中混有的NaCl杂质
(Ⅱ)回答下列问题:
(1)玻璃棒在实验中一般有如下三种用途:搅拌、引流和蘸取溶液,下列实验中至少用到其中两个用途的是______________________(填数字编号)。
①配制一定物质的量浓度的溶液 ②硫酸铜晶体结晶水含量的测定
③用硫酸铜和氢氧化钠制取氧化铜 ④从制取氧气的剩余固体中提取KCl
⑤测定溶液的pH ⑥浓盐酸与浓氨水相遇发烟
姓名: 班级: 成绩:
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
|
|
|
|
|
|
|
|
|
|
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
|
|
|
|
|
|
|
|
|
|
18.在浓度均为 3 mol/L 的盐酸和硫酸各100 mL溶液中,分别加入等质量的铁粉,充分反应后生成气体质量之比为 3∶4 。则加入铁粉的质量是 ( )
A.5.6 g B.8.4 g C.11.2 g D.1.8 g
第Ⅱ卷(非选择题 共76分)
17.几种短周期元素的原子半径及主要化合价如下表:
|
元素代号 |
L |
M |
Q |
R |
T |
|
原子半径/nm |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
|
主要化合价 |
+2 |
+3 |
+6、-2 |
+2 |
-2 |
下列叙述正确的是 ( )
A.R的氧化物对应的水化物可能具有两性 B.L、M的单质与稀盐酸反应速率:M > L
C.T、Q的氢化物常态下均为无色气体 D.L、Q形成的简单离子核外电子数相等
16.现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。甲、乙两元素相比较,可以验证金属性甲元素比乙元素较弱结论的实验是。 ( )
A.将在空气中放置已久的这两种元素的块状单质分别放入热水中
B.将这两种元素的单质粉末分别和同浓度的盐酸反应
C.将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
D.比较这两种元素的气态氢化物的稳定性
15.根据下表下列叙述中正确的是: ( )
|
序号 |
氧化剂 |
还原剂 |
其它反应物 |
氧化产物 |
还原产物 |
|
① |
Cl2 |
FeBr2 |
|
|
FeCl3 |
|
② |
KMnO4 |
H2O2 |
H2SO4 |
O2 |
MnSO4 |
|
③ |
KClO3 |
HCl(浓) |
|
Cl2 |
Cl2 |
|
④ |
KMnO4 |
HCl(浓) |
|
Cl2 |
MnCl2 |
A.表中第①组反应的氧化产物一定只有FeCl3(实为Fe3+)
B.氧化性比较: KMnO4>Cl2>Fe3+>Br2>Fe2+
C.还原性比较: H2O2>Mn2+>Cl-
D.④的离子方程式配平后,H+的化学计量数为16
14.下列反应的离子方程式正确的是 ( )
①硫酸铜溶液与氢氧化钡溶液反应: Ba2++ SO42_= BaSO4↓
②将金属钠加入水中 2Na + 2H2O = 2Na+ + 2OH - + H2 ↑
③石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+ Ca2++CO2↑+H2O
④氟气与水反应: F2+H2O=H+ +F -+ HFO
⑤小苏打溶液中加入少量的石灰水:Ca2+ +2OH-+2HCO3-=CaCO3↓+CO32- +2H2O
⑥次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO- + CO2 + H2O =CaCO3↓+ 2HClO
⑦钠与硫酸铜溶液反应:Cu2++2Na =2Na+ +Cu
⑧氯气与水反应Cl2 + H2O = 2H+ + Cl - + ClO-
⑨纯碱溶液中滴加少量盐酸CO32- + H+ = HCO3-
A.①②⑤⑨ B.②③⑤⑨ C.④⑤⑥⑦ D.②③⑧⑨
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com