
题目列表(包括答案和解析)
1.钠盐和钾盐性质相似,但在实际生产中多用钾盐而不用钠盐。如在实验室制氧气是用KClO3而不是用NaClO3,制黑火药用KNO3而不用NaNO3,并且在KNO3中不能含有NaNO3。对上述现象,以下解释合理的是
A.钠盐比钾盐更容易得到 B.钾盐的氧化性比钠盐弱
C.钾盐的熔点比钠盐高 D.钠盐的吸湿性比钾盐强
13。 2.24L
2.24L
11.(11分)(1)①沸腾炉 吸收塔(每空1分,共2分)
10.⑴镁(Mg) 防止金属离子(Mg2+)水解
⑵4NH3+5O2 4NO+6H2O C+4HNO3(浓)
4NO+6H2O C+4HNO3(浓) CO2↑+4NO2↑+2H2O
CO2↑+4NO2↑+2H2O
⑶2NH4++2e-=2NH3↑+H2↑(每小题2分,共10分)
9. (14分)[实验设计]方法一:B;Fe+H2SO4=FeSO4+H2↑、FeSO4+2NaOH=Fe(OH)2↓+Na2SO4、H2SO4+2NaOH=Na2SO4+2H2O 中和反应方程式不写不扣分
方法二:⑦、⑨或⑦、⑧、②。(每空1分,共6分)
[探究思考](1)(共3分)由于Fe(OH)2部分被氧化,混入少量的Fe(OH)3(1分)。
|
(2)(共3分,各1分)打开,发生,Fe(OH)2·nH2O= Fe(OH)2+ nH2O。
(3)(共2分)向Fe2+和Fe3+的混合液中加入NaOH溶液后,观察生成的沉淀的颜色是否为灰绿色(或者可以将Fe(OH)3和Fe(OH)2混合后观察其颜色。)(合理答案均给分)
12.(9分)将Na2O2>和NaHCO3固体混合物置于密闭容器中加充分反应,放出气体后冷却。加热时可能发生的反应如下:
2 Na2O2+2NaHCO3 2NaOH+2Na2CO3+O2↑
2NaOH+2Na2CO3+O2↑
2 Na2O2+4NaHCO3 4Na2CO3+O2↑+2H2O
4Na2CO3+O2↑+2H2O
2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
(1)若固体混合物的质量为m,反应后冷却再称其质量减少了△m。设NaHCO3、Na2O2的物质的量分别为a,b,试确定下列条件下△m的取值范围(用含m的代数式表示)。
①当a/b≤1时,△m取值范围是
②当1<a/b≤2时,△m取值范围是
③当a/b>2时,△m取值范围是
(2)若m=14.52g,△m=1.28g时,向反应后的残留固体内滴加2.00mol/L盐酸140.0mL,可产生标准状况下的气体 L。
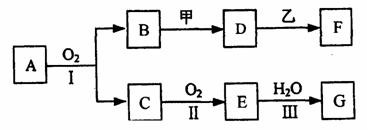
11.(11分)物质的转化关系如下图所示(有的反应可能在水溶液中进行)。其中A为化合物,甲可由两种单质直接化合得到,乙为金属单质,G为酸,乙在G的浓溶液中发生钝化。
(1)若A为黄色固体,C能使品红试液褪色,D的水溶液中加入HNO3酸化的AgNO3溶液有白色沉淀生成。则
①工业上反应I在 中进行,反应Ⅲ在 (均填设备名称)中进行。
②由两种单质直接化合得到甲的反应条件是 或 。
③反应I的化学方程式是 。
(2)若甲为淡黄色固体,D、F的溶液均呈碱性,用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近,有大量白烟生成。则①甲的电子式是 。
②D的溶液与乙反应的离子方程式是 。
③若1.7gA与O2反应生成气态的B和C时放出22.67kJ热量,写出该反应的热化学方程式:
10.(10分)已知A为中学化学中的常见金属,X、Y为常见非金属。X、E、F、G、J常温下为气体,C为无色液体,B是一种盐,受热易分解。现用A与石墨作电极,B的浓溶液作电解质,构成原电池。有关物质之间的转化关系如下图(部分反应的条件、生成物被略去):
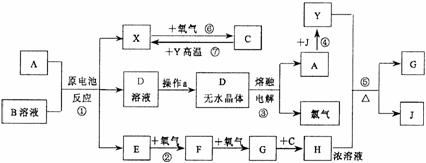
请填写下列空白:
⑴金属A为 ;操作a是将D溶液在HCl气流中蒸干,原因是
⑵反应②的化学方程式为: ;
反应⑤的化学方程式为: 。
⑶原电池反应①中,正极反应式为: 。
8.钡和钠相似,也能形成含O22-离子的过氧化物,下列叙述不正确的是
A.过氧化钡的化学式是Ba2O2
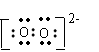 B.1 mol过氧化钡或过氧化钠跟足量的水反应都生成0.5 mol氧气
B.1 mol过氧化钡或过氧化钠跟足量的水反应都生成0.5 mol氧气
C.O22-离子的电子式为
D.过氧化钡或过氧化钠都是强氧化剂
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com