
题目列表(包括答案和解析)
24.(10分)将amolA(g)、dmolD(g)置于体积可变的密闭容器中加热至一定温度,发生如下反应:
2A(g)  2B(g)+C(g),2D(g)+C(g)
2B(g)+C(g),2D(g)+C(g)  2E(g)
2E(g)
t min时建立平衡,平衡时测得B的物质的量为mmol,C的物质的量为n mol,试求:
(1)平衡时,D的物质的量 (用d、m、n的代数式表示)
(2)平衡时若温度压强与反应前相同,则反应前和平衡时气体的密度之比为多少?(用含a、d、m、n的代数式表示)
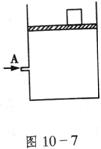
23.(8分)图10-7为一恒压容器。在恒定温度下,将1molN2和3molH2混合后由A口快速充入容器,封闭A,反应N2+H2 2NH3在t1时刻达到平衡,t2时刻再从A口快速充入一定量NH3,封闭A,t3时刻重新达平衡至t4。在图10-8画出0→t4时间段内混合气中NH3的体积分数(y坐标)随时间(x坐标)变化的曲线 。
2NH3在t1时刻达到平衡,t2时刻再从A口快速充入一定量NH3,封闭A,t3时刻重新达平衡至t4。在图10-8画出0→t4时间段内混合气中NH3的体积分数(y坐标)随时间(x坐标)变化的曲线 。

22.(12分)在537℃时,往容积可变的密闭容器中充入2molSO2(g)、1molO2(g),此时容器的体积为200L,压强为1.01×105Pa。向容器中加入固体催化剂,并保持恒温恒压,发生反应:2SO2+O2  2SO3,
2SO3,
达到平衡时,平衡气体中SO3的体积分数为0.91。试回答下列问题:
(1)从理论上看,压强增大,平衡向正反应方向移动,SO2的转化率增大。但工业上二氧化硫催化氧化采用常压而不用高压,主要的原因是 。
(2)保持上述温度和压强不变,若向容器中只充入2molSO3,并加入固体催化剂,则平衡时SO2的体积分数是 ,此时平衡混合气体的体积是 。
(3)温度仍保持537℃,容器的体积保持200L不变。充入amol SO2和bmolO2,并加入固体催化剂,反应达到平衡时,SO3的体积分数仍为0.91,体系压强为1.01×105Pa。若a:b=2:1,则a= 。
21.(9分)在一个容积固定的反应器中,有一可左右滑动的密封隔板两侧分别进行如图所示的可逆反应 :

各物质的起始加入量如下:A、B和C均为4.0mol,D为6.5mol、F为2.0mol,设E为xmol。当x在一定范围内变化时,均可以调节反应器的温度,使两侧反应均达到平衡,并且隔板恰好处于反应器的正中位置。请回答以下问题:
(1)若x等于4.5,则右侧反应在起始时向 方向移动,欲使起始反应维持向该方向进行,则x的最大取值范围是:
(2)若x分别为4.5和5.0时,则在这两种情况下,当反应达到平衡时,A的物质的量
(填“相等”或“不相等”)
20.(10分)t℃时,将3molA和2molB气体通入体积为2L的密闭容器中(容积不变),发生如下反应:3A(气)+B(气) 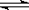 xC(气),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为O.4mol/L,请填写下列空白:
xC(气),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为O.4mol/L,请填写下列空白:
(1)x=__________。
(2)比较达到平衡时,A、B两反应物的转化率之比为α(A):α(B)= ;
(3)若继续向原平衡混合物的容器中通入少量氦气(氦气和A、B、C都不反应)后,下列说法中正确的是____________(填写字母序号)
A.化学平衡向正反应方向移动 B.化学平衡向逆反应方向移动
C.化学平衡不会发生移动 D.正、逆反应的化学反应速率保持不变
(4)在t℃时,若向原平衡混合物的容器中再充入amolC,欲使达到新的平衡时,各物质的物质的量分数与原平衡相同,则至少应再充入____ ______(填A或B)________mol(用a表示)。
19.(12分)在100℃时,将0.100mol的四氧化二氮气体充入1 L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如下数据:
 t/s t/sc/mol·L-1 |
0 |
20 |
40 |
60 |
80 |
100 |
|
c(N2O4)/mol·L-1 |
0.100 |
c1 |
0.050 |
C3 |
a |
b |
|
c(NO2)/mol·L-1 |
0.000 |
0.060 |
C2 |
0.120 |
0.120 |
0.120 |
试填空:
(1)该反应的化学方程式为________________ ______,达到平衡时四氧化二氮的转化率为_____ _,表中c2、c3、a、b大小关系为: 。
(2)20 s时四氧化二氮的浓度c1==____________mol·l-1,在0s-20s内四氧化二氮的平均反应速率为___________mol·(L·s)-1
(3)若在相同情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度是_________mol·L-1。
18.(10分)反应CaCO3 CaO+在不同温度下,CO2的平衡压强如下表:
CaO+在不同温度下,CO2的平衡压强如下表:
|
温度/℃ |
550 |
650 |
750 |
850 |
897 |
|
压强/Pa |
5.32×10 |
9.17×102 |
8.37×103 |
4.34×104 |
1.01×105 |
根据上表数据,填写下列空白:
(1)若升高原CaCO3的分解平衡体系的温度,同时给反应容器加压,则原平衡______。
A.向逆反应方向移动 B.向正反应方向移动
C.不移动 D.无法确定平衡移动方向
(2)在一个不与外界进行热交换的密闭器中足量的CaCO3在850℃时建立分解平衡。若将该容器的容积扩大为原来的2倍,需重新达到平衡时,容器内的温度将_______________,CaCO3的分解率将____________________________,CO2的平衡压强将________(填“>”、“=”、“<”)4.34×104Pa,其理由是_________________ ________________ ___
。
17.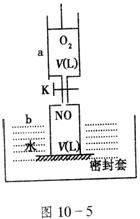 (12分)如图10-5(a中活塞的质量与筒壁的摩擦力不计;与K相连的细管的体积也忽略不计)。在标准状况下:
(12分)如图10-5(a中活塞的质量与筒壁的摩擦力不计;与K相连的细管的体积也忽略不计)。在标准状况下:
(1)b中气体与水不接触,打开K,足够长时间后,a中气体体积减少范围是:___________△V(减小)___________。
(2)在上述(1)之后,快速推a中活塞至a中气体全部进入b中,观察到的现象是_________________________,原因是____________________________________________。
(3)若固定a中活塞如图10-5所示,打开K,移走b的密封套,足够长时间后,观察到的现象是___________________________
_________________________________________________,所得溶质的物质的量浓度为(设溶质不扩散到水槽中)__________________。
16.在一固定容积的密闭容器中,加入m mol A、n mol B,发生下列反应:mA(g)+nB(g)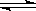 pC(g) 平衡时C的浓度是wmol/L,若容器体积和温度不变,起始时放入a mol A、b mol B、c mol C,若要平衡后C的浓度仍为wmol/L,则a、b、c应满足的关系是( )
pC(g) 平衡时C的浓度是wmol/L,若容器体积和温度不变,起始时放入a mol A、b mol B、c mol C,若要平衡后C的浓度仍为wmol/L,则a、b、c应满足的关系是( )
A.a︰b︰c=m︰n︰p B.a︰b=m︰n (ap/m)+c=p
C.(mc/p)+a=m,(nc/p)+b=n D.a=m/3,b=n/3,c=2p/3
(第Ⅱ卷共86分)
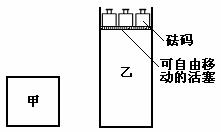
15.一定温度下,有可逆反应:2A(g)+2B(g) C(g)+3D(g);ΔH<0。现将2 mol A和2 mol B充入体积为V的甲容器,将2 mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。
C(g)+3D(g);ΔH<0。现将2 mol A和2 mol B充入体积为V的甲容器,将2 mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。
|
关于两容器中反应的说法正确的是
A.甲容器中的反应先达到化学平衡状态
B.两容器中的反应均达平衡时,平衡混合物中各组份的体积百分组成相同,混合气体的平均相对分子质量也相同
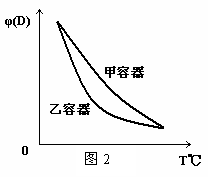
C.两容器达平衡后升高相同温度,两容器中物质D的体积分数随温度变化如图2 所示
D.在甲容器中再充入2 mol A和2 mol B,平衡后甲中物质C的浓度是乙中物质C的浓度的2倍
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com