
题目列表(包括答案和解析)
2.“神六”问题--肼(N2H4)、偏二甲肼((C2H5)2N-NH2)
1.05年诺贝尔化学奖烯烃复分反应
3.运用基本操作合成新物质
3.除杂试剂选择与顺序→食盐精制
 1.将课本反应设计成实验
1.将课本反应设计成实验
C.实验综合题 2.将课本实验细化研究
7.实验安全考核
 1.多种鉴别方法
1.多种鉴别方法
B.实验设计题 2.验证Na2SO3. H2O2. Na2NO2的氧还性
①试题的难度系数在0.55-0.65之间 ②题型以稳为主,稳中求变,变中求新,新中求活。
Ⅰ卷目的:主要考查双基,覆盖知识面,平衡整卷均分。
试题指向:
⑴ 环境化学 (围绕酸雨、臭氧、温室效应、光化学烟雾出题)
⑵ 氧化还原(以概念、氧化性还原性强弱判断、电子守恒法计算为重点)
⑶ 化学研究前沿 (围绕绿色化学、原子经济性、纳米材料、新材料研究)
⑷ NA的考查(以物质的量为中心,气体摩尔体积概念及阿氏定律的理解,联系电解质溶液知识,以及物质结构知识)
⑸ 溶液浓度的考查 (物质的量浓度与质量分数、溶解度间的换算,溶液混和与密度的关系)
⑹ 离子共存 (注意各种各样的条件限制) ;
⑺.离子方程式判断 (注意量的制约)
⑻.热化学的考查 (重点热化学方程式书写、燃烧热的定义与计算)
⑼.原子结构,核组成符号含义 (以新元素的发现,新微粒的重大用途为背景出题)
⑽.周期律 (判断未知元素可能性质); 周期表(X、Y元素原子序数之差,位构性三者关系)
⑾.分子结构 (以键极性、分子极性、分子形状、是否满足8e结构展开出题)
⑿.晶体结构 (重在判断各类晶体与性质的内在联系)
⒀.速率平衡 (平衡状态判断、平衡移动方向、图象分析、转化率大小判断等常考常新)
⒁ pH值计算 (以强酸、强碱稀释类、混和类为主)
⒂.离子浓度大小比较 (以典型溶液为主;物料守恒、电荷守恒为难点)
⒃.电化学 (电极反应式书写、电解产物判断与计算、实用电池分析)
⒄.元素性质 (突出半径、熔沸点、密度大小比较以及稳定性、酸碱性等递变规律)
⒅.有机化学 (原子线、面分析、异构体数判断、官能团结构与性质关系、反应类型是热点)
⒆.基本操作 (围绕药品保存、仪器选用、仪器清洗、鉴别、分离、实验误差等问题考查)
⒇化学计算 (以差减法、平均法、极限法、守恒法为主)
II卷目的:主要考查能力,内容体现基础性+综合性,形式体现旧知性+新信息,设问体现阶梯性+灵活性。
试题指向:
实验题:第1题为基础题A型;第2题拉分题B、C型。突出实验设计与评价,重在旧知迁移,强化思维的逻辑性和表达的规范性。
 1.基本仪器及基本操作 2.读数的方法与数据
1.基本仪器及基本操作 2.读数的方法与数据
A.实验操作题 3.试剂配制方法 4.鉴别操作→干扰排除
5.除杂操作 6.PH测定,焰色反应等
28.(19分)
I. 合成氨工业对化学的国防工业具有重要意义。写出氨的两种重要用途 、
。
II. 实验室制备氨气,下列方法中适宜选用的是 。
① 固态氯化铵加热分解 ② 固体氢氧化钠中滴加浓氨水
③ 氯化铵溶液与氢氧化钠溶液共热 ④ 固态氯化铵与氢氧化钙混合加热
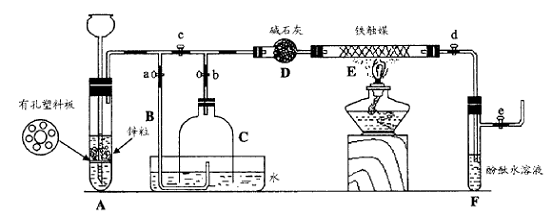
III. 为了在实验室利用工业原料制备少量氨气,有人设计了如下装置(图中夹持装置均已略去)。
[实验操作]
① 检查实验装置的气密性后,关闭弹簧夹a、b、c、d、e。在A中加入锌粒,向长颈漏斗注入一定量稀硫酸。打开弹簧夹c、d、e,则A中有氢气发生。在F出口处收集氢气并检验其纯度。
② 关闭弹簧夹c,取下截去底部的细口瓶C,打开弹簧夹a,将氢气经导管B验纯后点燃,然后立即罩上无底细口瓶C,塞紧瓶塞,如图所示。氢气继续在瓶内燃烧,几分钟后火焰熄灭。
③ 用酒精灯加热反应管E,继续通氢气,待无底细口瓶C内水位下降到液面保持不变时,打开弹簧夹b,无底细口瓶C内气体经D进入反应管E,片刻后F中的溶液变红。
回答下列问题:
(1)检验氢气纯度的目的是 。
(2)C瓶内水位下降到液面保持不变时,A装置内发生的现象是 ,防止了实验装置中压强过大。此时再打开弹簧夹b的原因是 ,C瓶内气体的成份是 。
(3)在步骤③中,先加热铁触媒的原因是 。
反应管E中发生反应的化学方程式是 。
28.(19分)烯烃通过臭氧化并经锌和水处理得到醛或酮。例如:
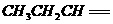
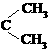
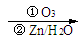
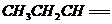


I. 已知丙醛的燃烧热为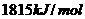 ,丙酮的燃烧热为
,丙酮的燃烧热为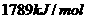 ,试写出丙醛燃烧的热
,试写出丙醛燃烧的热
化学方程式 。
II. 上述反应可用来推断烯烃的结构。一种链状单烯烃A通过臭氧化并经锌和水处理得到B和C。化合物B含碳69.8%,含氢11.6%,B无银镜反应,催化加氢生成D。D在浓硫酸存在下加热,可得到能使溴水褪色且只有一种结构的物质E。反应图示如下:
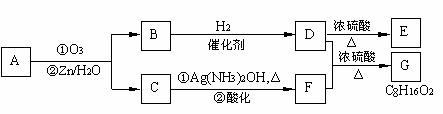
回答下列问题:
(1)B的相对分子质量是
;C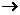 F的反应类型为
;D中含有官能团的名称
。
F的反应类型为
;D中含有官能团的名称
。
(2)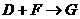 的化学方程式是:
的化学方程式是:
。
(3)A的结构简式为 。
(4)化合物A的某种同分异构体通过臭氧化并经锌和水处理只得到一种产物,符合该条件的异构体的结构简式有 种。
27.(9分)A、B、C、D是短周期的四种元素,其原子序数依次增大。已知A、D同主族,C、D同周期,A原子L层电子数是K层电子数的2倍,B原子最外层有6个电子,且A原子和D原子的最外层电子数之和等于B原子和C原子的最外层电子数之和。请用化学用语回答以下问题:
(1)A、D两种元素分别是 、 。(写元素符号)
(2)A、B、C、D原子半径由小到大的顺序 。
(3)写出由上述元素组成的单质化合物之间相互作用发生置换反应的一个化学方式:
。
(4)B和C两元素组成的化合物在固态时属于 晶体(填晶体的类型),其电子式
为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com