
题目列表(包括答案和解析)
1、下列有关硅及其化合物的叙述中,错误的是 [ ]
A.硅原子有4个价电子,能够形成4个共价键
B.硅晶体结构跟金刚石的结构相似,也是一种原子晶体
D.硅酸、原硅酸和由它们缩水结合而成的各种酸所对应的盐,统称硅酸盐
26.据材料称:钠可在氮气中燃烧生成氮化钠,氮化钠与水反应的化学方程式是:
Na3N+4H2O==3NaOH+NH3·H2O。某学校化学研究学习小组,为了研究钠在空气中燃烧产物的成分,做了以下实验:
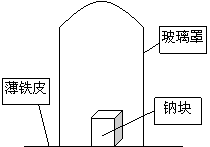 取11.5g钠单质放在一块薄铁皮上,上扣一玻璃罩(玻璃罩内为干燥且无酸性气体的空气),用酒精灯加热薄铁皮,钠完全燃烧,将燃烧产物投入水中,得到一种纯净气体0.224L(标准状态)和1000mL溶液,从中取出25.00mL溶液,和13.50mL 1.00mol·L-1HCl溶液刚好完全反应。求钠在空气中燃烧产物的成分及物质的量。
取11.5g钠单质放在一块薄铁皮上,上扣一玻璃罩(玻璃罩内为干燥且无酸性气体的空气),用酒精灯加热薄铁皮,钠完全燃烧,将燃烧产物投入水中,得到一种纯净气体0.224L(标准状态)和1000mL溶液,从中取出25.00mL溶液,和13.50mL 1.00mol·L-1HCl溶液刚好完全反应。求钠在空气中燃烧产物的成分及物质的量。
高三化学下学期期初考试试题
25.2.80g铁与100mL稀硝酸混合后充分反应,产生气体为NO,反应后铁、硝酸均无剩余。向反应后的溶液中加入100mL0.2mol/L的碘化钾溶液,恰好将溶液中的Fe3+全部还原。求原硝酸溶液的物质的量浓度?
24.据报导,目前我国结核病的发病率有抬头的趋势。抑制结核杆菌的药物除雷米封外,PAS-Na(对氨基水杨酸钠)也是其中一种。它与雷米封可同时服用,可以产生协同作用。已知:
①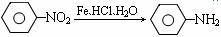 (苯胺、弱碱性、易氧化)
(苯胺、弱碱性、易氧化)
②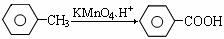
下面是PAS-Na的一种合成路线(部分反应的条件未注明):
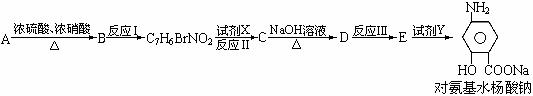
按要求回答问题:
⑴写出下列物质的结构简式:C:____________________D:______________________;⑵写出下列反应的化学方程式并配平
A→B:__________________________________________________________________;
B→C7H6BrNO2:__________________________________________________________;
⑶指出反应类型:I_________________,II_________________;
⑷指出所加试剂名称:X______________________,Y____________________。
23.有机物A与乙酸无论以何种比例混合,只要质量一定,完全燃烧后产生的水的质量也一定,试回答:
⑴若A与乙酸相对分子质量相等,且既能发生银镜反应又能发生酯化反应,则A的结构简式为_____________。
⑵若A由四种元素形成的两种官能团组成,相对分子质量与乙酸相等,且分子中氢原子都不与碳原子相连,则A的结构简式为_____________。
⑶若A分子中C、H元素质量分数之和为86.67%,其余为O,且A的相对分子质量小于200,则A的分子式为___________。如果A分子每个碳原子都达到饱和,且能与金属钠反应产生氢气,则A的结构简式为________________________。
22.(1)周期表中前20号元素中有A、B、C、D、E五种元素。已知它们都不是稀有气体元素,且原子半径依次减小,其中A和E同族,A与C、B与E原子的电子层数都相差2。A、B原子最外层电子数之比为1∶4。A和C能以原子个 数比1∶1形成化合物。
①写出元素符号 A B D E
②B与D形成的化合物是 分子(填极性、非极性)。
③用电子式表示A和D形成化合物过程
(2) 1183 K以下纯铁晶体的基本结构单元如图1所示,1183 K以上转变为图2所示结构的基本结构单元,在两种晶体中最邻近的铁原子间距离相同。
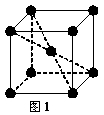
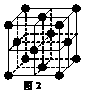
①在1183 K以下的纯铁晶体中,与铁原子等距离且最近的铁原子数为_______个;在1183 K以上的纯铁晶体中,与铁原子等距离且最近的铁原子数为___________;
②纯铁晶体在晶型转变前后,二者基本结构单元的边长之比为(1183 K以下与1183 K以上之比)___________。
③转变温度前后两者的密度比(1183 K以下与1183 K以上之比)_____________。
21. 已知A、B、E是固体化合物,D、G是固体单质,X、Z、F为可燃性气体,F、X的火焰呈淡蓝色,他们之间有如下转化关系:
已知A、B、E是固体化合物,D、G是固体单质,X、Z、F为可燃性气体,F、X的火焰呈淡蓝色,他们之间有如下转化关系:
⑴写出A、B、Z的名称:A ,B ,Z
⑵写出Y的结构式: ,A的晶体结构类型: ,
溶液H的保存要求 ;
⑶按要求写出反应方程式:
①的化学方程式:
⑥离子方程式:
20.向溴水中加入足量的乙醛溶液,可以看到溴水褪色,对产生该现象的原因有如下三种猜想:①溴水与乙醛发生取代反应;②由于乙醛分子中有不饱和键,溴水与乙醛发生加成反应;③由于乙醛具有还原性,溴水将乙醛氧化为乙酸。为探究哪种猜想正确,一研究性学习小组提出了如下两种实验方案:
方案一:检验褪色后溶液的酸碱性;
方案二:测定反应前溴水中Br2的物质的量和反应后溶液中Br-离子的物质的量。
⑴方案一是否可行 (填“是”或“否”),理由是 。
⑵假设测得反应前溴水中Br2的物质的量为amol,若测得反应后n(Br-)= mol,则说明溴水与乙醛发生取代反应;若测得反应后n(Br-)= mol,则说明溴水与乙醛发生加成反应;若测得反应后n(Br-)= mol,则说明溴水将乙醛氧化为乙酸。
⑶按物质的量之比为1:5配制1000mLKBrO3-KBr溶液,该溶液在酸性条件下完全反应可生成0.5molBr2。 取该溶液10mL加入足量乙醛溶液,使其褪色,然后将所得溶液稀释为100mL,准确量取其中10mL,加入过量的AgNO3溶液,过滤、洗涤、干燥后称量得到固体0.188g。若已知CH3COOAg易溶于水,试通过计算判断溴水与乙醛发生反应的类型为 (选填猜想序号)。
⑷写出上述测定过程中的三个反应的离子方程式:
①KBrO3和KBr在酸性条件下的反应 : ;
②溴水与乙醛的反应: ;
③测定Br-离子含量的反应: ;
19.有常用玻璃仪器组成的下列五种实验装置(根据需要可在其中加入液体或固体)
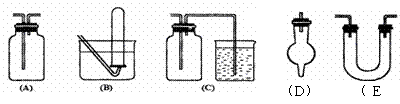
(1)能用做干燥二氧化硫气体的装置有________(填代号,下同)
(2)既能用于收集氯气又能用于收集一氧化氮气体的装置有________
(3)在氯气和铁反应实验中,能添加在制气和化合反应装置之间以除去氯气中氯化氢
等杂质气体的装置有________
(4)若用C装置做二氧化硫与烧杯中氢氧化钠溶液反应实验,则其中广口瓶的作用是________.
18.已知400℃和1标准大气压时的气体摩尔体积为55.20L/mol,在该条件下1mol气体发生如下反应并达到平衡:2X(g) mY(g) + Z(g) ,测得混合气体中X的体积分数为0.5880,混合气体的总质量为46.00克,混合气体的密度为0.72g/L 。则平衡混合气体的平均相对分子质量为( )
 A.58.80 B.46.00 C.39.72 D.16.13
A.58.80 B.46.00 C.39.72 D.16.13
第Ⅱ卷 (非选择题 共76分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com