
题目列表(包括答案和解析)
7.将两个铂电极插入500毫升CuSO4溶液中进行电解, 通电一定时间后, 某一电极增重0.064克(设电解时该电极无氢气析出, 且不考虑水解和溶液体积变化). 此时溶液中氢离子浓度约为( )
A.4×10-3mol/L B.2×10-3 mol/L
C.3×10-3 mol/L D.1×10-3 mol/L
6.在恒温、恒容的密闭容器中进行反应 A(g)===B(g)+C(g),若反应物的浓度由2 mol·L-1降到0.8 mol·L-1需要20 s,那么反应物浓度再由0.8 mol·L-1降到0.2 mol·L-1所需要的时间为( )
A.10 s B.大于10 s C.小于10 s D.无法判断
5.表示下列变化的化学用语正确的是( )
A.NaHCO3的水解:HCO3-+H2O H3O+ +CO32-
H3O+ +CO32-
B.金属铝溶于NaOH溶液:Al+2OH-=AlO2-+H2↑
C.钢铁吸氧腐蚀的正极反应式:4OH--4e-=O2+2H2O
D.1 L0.5 mol·L-1稀硫酸与1 L1 mol·L-1 NaOH溶液反应放出57.3 kJ的热:
H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l);△H=-114.6 kJ/mol
4.将铁和铝的混和粉未溶于过量盐酸中,通入足量氯气,再加入过量的NaOH溶液,最后溶液中大量存在的离子是( )
A.Na+ Fe2+ Cl- AlO2- B.Na+ Fe3+ Cl- OH-
C.Na+ Fe3+ Cl- AlO2- D.Na+ Cl- OH- AlO2-
3.现有4mol铝及足量稀HCl和稀NaOH溶液,欲将铝全部转化为Al(OH)3,所需HCl与NaOH的物质的量之和最少应是( )
A.6mol B.4mol C.16mol D.8mol
2.在FeCl3溶液中滴加无色的KSCN溶液后有以下可逆反应:FeCl3+3KSCN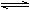 Fe(SCN)3+3KCl,已知Fe(SCN)3呈红色,则在该平衡体系中加少量KCl固体后,红色将( )
Fe(SCN)3+3KCl,已知Fe(SCN)3呈红色,则在该平衡体系中加少量KCl固体后,红色将( )
A.变深 B.变浅 C.不变 D.无法确定
1.近年来,冠以“绿色”的新概念不断产生。“绿色化学”要求从经济、环保和技术上设计可行的化学反应。据此,由单质镁制硝酸镁的下列4个方案中,你认为可行而且符合“绿色化学”要求的方案是( )
A.Mg Mg(NO3)2
Mg(NO3)2
B.Mg MgCl2
MgCl2 Mg(OH)2
Mg(OH)2 Mg(NO3)2
Mg(NO3)2
C.Mg MgO
MgO Mg(NO3)2
Mg(NO3)2
D.Mg MgSO4
MgSO4 Mg(NO3)2
Mg(NO3)2
2.24克铁与100mL稀硝酸混合后充分反应,还原产生只有NO,并且铁、硝酸均无剩余。向反应后溶液中加入50mL0.2mol·L-1的KI溶液,恰好将溶液中的Fe3+全部还原。求原硝酸溶液的物质的量浓度。
(15分)PMAA是一种“智能型”有机高分子化合物,可应用于生物制药中大分子和小分子的分离。可以用下面的设计方案合成:
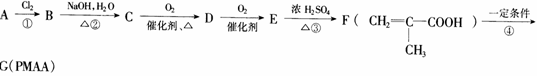
请填写下列空白:
(1)与出A、G的结构简式:A:_________________________,G:_______________________。
(2)①②③④反应中属于取代反应的有_________________________。
(3)写出C D的化学方程式:___________________________。
D的化学方程式:___________________________。
(4)C与F在浓硫酸存在和加热条件下能够充分反应,此反应的反应类型是___________________,1 mol C最多能与___________________(填物质的量)F完全反应。
19、在一定条件下,NO2跟NH3可以发生反应生成N2和H2O。现有NO2与NH3的混合物Imol,充分反应后所得产物中,经氧化得到的N2比经还原得到的N2多1.4g。
(1)写出反应的化学方程式并标出电子转移的方向和数目。
(2)若以上反应进行完全,试计算原反应混合物中NO2与NH3的物质的量可能各是多少。
2、某一无色透明溶液中可能存在H+ 、Ba2+、Mg2+ 、Cu2+ 、OH- 、HCO3- 、SO32-、NO3- 、Cl-中的一种或几种。已知该溶液能与Al反应放出H2 。 (1)若反应生成Al3+,则原溶液中一定存在或可能存在的离子有 _______________________ 。 (2)若反应生成AlO2- ,则原溶液中一定存在或可能存在的离子有 ______________________ 。
*3.已知Cl2通入浓氨水中会发生如下反应:3Cl2+8NH3=6NH4Cl+N2,今有体积为1.12L,质量为3.335g的Cl2和N2的混合气体通过浓氨水后,体积变为0.672L[其中Cl2、N2各占50%(体积分数)]。(气体体积均在标准状况下测定)
(1)经计算,被氧化的氨的质量为___ _g。(不必写出计算过程)
(2)下面是三位学生从不同角度解这道题时所列的第一步算式,请判断他们所列未知数x分别表示什么量,并填写在表格内:
|
学生编号 |
所列第一步算式 |
未知数x表示的意义 |
|
甲 |
(3-1)∶2=(1.12-0.672)/22.4∶x |
|
|
乙 |
3∶(x-0.672/2)=1∶[0.672/2-(1.12-x)] |
|
|
丙 |
71x+28(1-x)=3.335/1.12×22.4 |
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com