
题目列表(包括答案和解析)
19.(10分)请按要求填空
⑴下列实验操作或对实验事实的叙述正确的是 (填序号)。
①向试管中滴加液体时,为不使液体滴到试管外应将胶头滴管伸入试管中;
②一小块金属钠加入水中后迅速熔成小球,不停地在水面游动并发出“吱吱”的响声;
③配置100mL1.00mol/L的NaCl溶液时,可用托盘天平称取5.85g NaCl固体;
 ④向可能含有SO42-、SO32-的溶液中加入过量的盐酸,再加入Ba(NO3)2溶液,可检验SO42-的存在;
④向可能含有SO42-、SO32-的溶液中加入过量的盐酸,再加入Ba(NO3)2溶液,可检验SO42-的存在;
⑤蒸发NaCl溶液以得到NaCl固体时,不必将溶液蒸干;
⑥向100℃时的NaOH稀溶液中滴加饱和的FeCl3溶液,以制备
Fe(OH)3胶体;
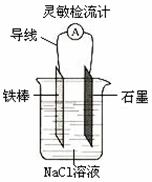
⑦如右图,可观察到灵敏检流计的指针偏转;
⑧向AlCl3溶液中滴加NaOH溶液和向NaOH溶液中滴加AlCl3溶
液的现象相同。
⑵现有0.1mol·L-1的纯碱溶液,用pH试纸测定该溶液的pH,其
正确的操作是 ① 。你认为该溶液pH的范围一定介于 ② 之间。请你设计一个简单的实验方案证明纯碱溶液呈碱性是由CO32-引起的: ③ 。
18、将16 g FeS与FeO的混合物,投入到含有1 mol的硝酸溶液中充分反应,只产生1/3 mol NO气体,得到澄清的混合溶液,下列计算结果正确的是
A.混合物中含有8 g FeO
B.混合物中含有0.1 mol FeS
C.被还原的HNO3 为1/3 mol
D.参加反应的HNO3 为1 mol
班级____________ 学号___________ 姓名______________
第I卷(选择题,共74分)
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
|
|
|
|
|
|
|
|
|
|
|
第Ⅱ卷(非选择题,共76分)
17、原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中不正确的是
A.由Al、Cu、稀H2SO4组成原电池,其负极反应式为:Al-3e-=Al3+
B.由Mg、Al、NaOH溶液组成原电池,其负极反应式为:
Al-3e-+4OH-=AlO2-+2H2O
C.由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu-2e-=Cu2+
D.由Al、Cu、浓硝酸组成原电池,其负极反应式为:Cu-2e-=Cu2+
16、将某些化学知识用数轴表示,可以收到直观现象、简明易记的效果。用数轴表示的下列化学知识中不正确的是
A. 常温条件下,酚酞的变色范围:
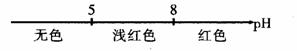
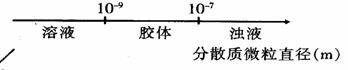
B. 分散系的分类:
C. AlCl3和NaOH溶液反应后铝元素的存在形式:
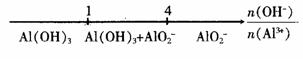
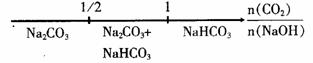
D. CO2与NaOH溶液反应的产物:
15、在铜的催化作用下氨气和氟气反应,得到一种三角锥形分子M和一种盐N。下列有关说法正确的是
A.该反应中氨气和氟气的化学计量数之比为4∶3
B.该反应的还原产物是M
C.M是极性分子,其还原性比NH3强
D.N中只有一种化学键
14、 我国科学家合成出世界上最细的碳纳米管,直径仅有0.5nm,与C36分子直径相当。已知C36是由正五边形和正六边形构成的足球分子,在多面体中,棱边数=顶点数+面数-2。根据以上信息,下列有关推断不正确的是
A. 碳纳米管与金刚石互为同素异形体
B.这种碳纳米材料分散到适当分散剂中,一定能形成胶体
C.每个C36分子中有18个双键
D.C36分子中有12个正五边形,8个正六边形构成
13、有许多非金属氧化物在一定条件下都能与Na2O2反应,且反应极有规律。如:2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+SO3=2Na2SO4+O2。据此,你认为下列反应方程式中正确的是
A. 2Na2O2+2SO2=2Na2SO3+O2 B. Na2O2+2NO2=2NaNO2+O2
C. 2Na2O2+2Mn2O7=4NaMnO4+O2 D. 2Na2O2+2N2O5=4NaNO3+O2
12、NA代表阿伏加德罗常数,下列说法正确的是
A. 在合成氨的平衡体系中,有1molN≡N键断裂,必有6NA个N-H键同时断裂
B. 中子数为1.5NA的重水(D216O)的质量为3g
C. 64g铜与足量的硫反应失去2NA个电子
D. 1L1mol/L的氢氟酸中含NA个氢离子
11、某溶液含有大量Ag+、NH4+、Al3+、Fe2+四种离子。往该溶液中加入足量Na2O2,充分搅拌后,再加入过量稀盐酸,此时溶液中一定能大量存在的离子是
A.Na+、NH4+、OH- B. Fe2+、Al3+、Cl-
C. Na+、Fe3+、Al3+ D. Ag+、Fe3+、NH4+
10、下列离子方程式正确的是
A.等物质的量的NH4HCO3与NaOH在溶液中反应:
NH4++HCO3-+2OH-=CO32-+NH3↑+2H2O
B.在蓝色的淀粉溶液中通入足量SO2后成无色溶液:
I2+SO2+2H2O=2I-+SO42-+4H+
C.四氧化铁粉末溶于足量的稀HNO3:
Fe3O4+8H+=2Fe2++Fe3++4H2O
D.向Ca(ClO)2溶液中通入足量的CO2气体:
Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com