
题目列表(包括答案和解析)
32、某待测液中可能含有Fe2+、Fe3+、Ag+、Al3+、Ba2+、NH 4+
等离子,进行如下实验(所加酸、碱、氨水、溴水都是过量的)。
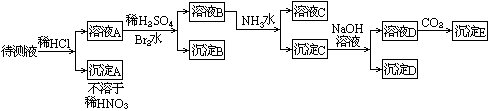 根据实验结果:
根据实验结果:
(1)溶液中一定存在的离子是:
(2)写出沉淀B的分子式: ,沉淀D的分子式:
(3)写出从溶液D生成沉淀E反应的离子方程式:
________________________________
31、粉状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验:
①取适量的A进行铝热反应,产物中有单质B生成
②另取20gA全部溶于0.15L6.0mol/L的盐酸中,得溶液C
③将①中得到的单质B和溶液C反应,放出1.12L(标况)气体,同时生成溶液D,还残留有物质B;④用KSCN溶液检验时,溶液D不变色
请填空:(1)①中引发铝热反应的实验操作是
。
产物中的单质B是(化学式) 。
(2)②中发生的各反应的方程式是
。
(3)③中发生的各反应的离子方程式是
。
(4)若溶液D的体积视为0.15L,则该溶液中C(Mg2+)为_____________,
C(Fe2+)为_____________。
30、某同学两次用2.6 g Zn和稀HNO3反应,两次所用的溶液中均含有6.3 g HNO3,但浓度不同,又知第一次实验中有1/5 HNO3被还原,第二次实验中只有1/10 HNO3被还原,试写出相应的化学反应方程式
第一次 。
第二次 。
29、2.3 g某液态有机物和一定量的氧气混合点燃,恰好完全燃烧,生成2.7 g水(液态)和2.24 L CO2(标况)并放出68.35 kJ热量,则该反应的热化学方程式为
。
28、NaBH4作为还原剂,在有机化学中有极为广泛的用途。.
(1)NaBH4极易溶解于水并与水作用产生H2,反应后硼元素以BO2-形式存在于溶液中,此反应的离子方程式是 。 (2)该反应与溶液酸碱度有关,PH越小,反应速率越______理由是 。
(3)NaBH4可使许多金属离子还原为金属单质,例如它可以使含有金离子(Au3+)的废液中Au3+还原(碱性条件,此时硼仍然以BO2-形式存在),离子方程式是
。
27、已知:①P4(s、白磷)+5O2(g)===P4O10(s);ΔH= -2983.2 kJ·mol-1
②P(s、红磷)+ O2(g)=
O2(g)=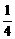 P4O10(s);ΔH=-738.5
kJ·mol-1,试写出白磷转化为红磷的热化学方程式
。
P4O10(s);ΔH=-738.5
kJ·mol-1,试写出白磷转化为红磷的热化学方程式
。
26、有甲、乙、丙、丁4种液体,它们分别是Fe(OH)3胶体、硅酸溶胶、As2S3胶体、NaOH溶液。现将有关试验现象记录如下:(1)电泳:甲液体的阳极周围颜色变浅,阴极周围颜色变深;(2)将一束光通过乙液体,无丁达尔现象;(3)将乙慢慢加入到丙液中,先出现聚沉,后液体变清。则甲为__________;乙为__________;丙为____________;
丁为____________。
25、下列各组物质,在只有水和试管的条件下,达不到鉴别目的的是( )
A、硝基苯、乙醇、乙酸乙酯
B、Na2O2、CaCl2、CuSO4、
C、CaCO3、NaHSO4、CaC2、Mg(OH)2
D、KCl、Na2SO4、AlC13、Mg3N2
第Ⅱ卷:非选择题(共58分)
24、在反应:11P+15CuSO4+24H2O===5Cu3P+6H3PO4+15H2SO4中,7.5 mol CuSO4可氧化磷原子的物质的量为( )
A、1.5 mol B、3 mol C、5 mol D、6 mol
23、下列说法正确的是( )
A、金属的导电过程是物理变化
B、晶体中有阳离子时必有阴离子
C、金刚石、铝、氖等物质的晶体都是由原子组成的
D、二氧化硅、二氧化碳的晶体内都存在化学键
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com