
题目列表(包括答案和解析)
7.向某溶液加入BaCl2溶液后无沉淀,再向该溶液中加入NaOH溶液出现了白色沉淀,则原溶液中可能存在的阴离子是
A.HSO4- B.HCO3- C.NO3- D.Cl-
6.t℃时,将溶质质量分数为a %的NaOH溶液蒸发掉m g水后恢复至原温度,恰好得到质量分数为2a %的NaOH饱和溶液V mL,则下列说法中正确的是
A.t℃时NaOH的溶解度为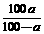 g
g
B.原溶液的质量为2m g
C.原溶液的物质的量浓度为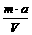 mol·L-1
mol·L-1
D.保持t℃,向原溶液中加入2a gNaOH可达饱和
5. 下列化学实验的方案正确的是
下列化学实验的方案正确的是
A.配制银氨溶液:将浓氨水逐滴加入到稀的硝酸银
溶液中至生成沉淀刚好溶解
B.分离苯和苯酚:加入适量的浓溴水,过滤
C.实验室用二氧化锰与浓盐酸制氯气可用右图装置实现
D.除去溴乙烷中含有的少量溴:加入亚硫酸钠溶液,充分振荡后分液
4.肼(N2H4)是火箭发动机的燃料,反应时N2O4为氧化剂,生成氮气和水蒸气。已知:
N2(g)+2O2(g)=N2O4(g);△H= +8.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-534.0kJ/mol
下列表示肼跟N2O4反应的热化学方程式,正确的是
A.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-542.7kJ/mol
B.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-1059.3kJ/mol
C.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-1076.7kJ/mol
D.N2H4(g)+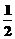 N2O4(g)=
N2O4(g)=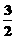 N2(g)+2H2O(g);△H=-1076.7kJ/mol
N2(g)+2H2O(g);△H=-1076.7kJ/mol
3. 氮化碳结构如右图,其中β-氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料。下列有关氮化碳的说法不正确的是
氮化碳结构如右图,其中β-氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料。下列有关氮化碳的说法不正确的是
A.氮化碳属于原子晶体
B.氮化碳中碳显-4价,氮显+3价
C.氮化碳的化学式为:C3N4
D.每个碳原子与四个氮原子相连,每个氮原子与三个碳原子相连
2.希尔实验是将分离出的叶绿素加到草酸铁溶液中,经光照后发生反应:4Fe3++2H2O光照叶绿体4Fe2++4H++O2↑,下列有关该实验的说法正确的是
A.反应后溶液的pH上升 B.每生成1 mol O2转移2 mol电子
C.叶绿体在反应过程中被氧化 D.该实验可说明光合作用产生的氧气来源于水
1.下列有关化学与生活相关说法正确的是
A.为防止食品氧化变质,常在包装袋中放人生石灰
B.压缩天然气和液化石油气是两类常见的清洁燃料,属于碳氢化合物
C. 福尔马林是一种良好的杀毒剂,也可用来消毒自来水
D.使用加酶洗衣粉时,水温越高,洗涤效果越好
31.(6分)现有6.95 g Fe、Al混合物溶解在200 mL某浓度的稀硝酸中。当金属粉末完全溶解时,收集到3.36L 的NO气体(标准状况)。在反应后的溶液中逐滴加入
2 mol·L-1的NaOH溶液,生成沉淀的质量与加入NaOH溶液体积的关系如下图所示。试求:
(1)沉淀的最大质量。
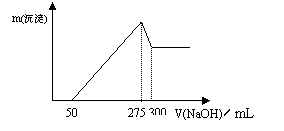
(2)原稀硝酸的物质的量浓度。
30.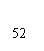 (4分)酒度是指酒中所含乙醇的体积百分比,如 (1%)酒是1体积乙醇和99体积水的混合溶液。已知水和乙醇的密度分别为1.0g·cm-3和0.8g·cm-3。试计算 (52%)“德山大曲”白酒中乙醇的质量分数。
(4分)酒度是指酒中所含乙醇的体积百分比,如 (1%)酒是1体积乙醇和99体积水的混合溶液。已知水和乙醇的密度分别为1.0g·cm-3和0.8g·cm-3。试计算 (52%)“德山大曲”白酒中乙醇的质量分数。
29.(6分)用石油裂解得到的乙烯和1,3-丁二烯为原料,经过下列途径合成高分子化合物E。E可用于制造以玻璃纤维为填料的增强塑料(俗称玻璃钢)。
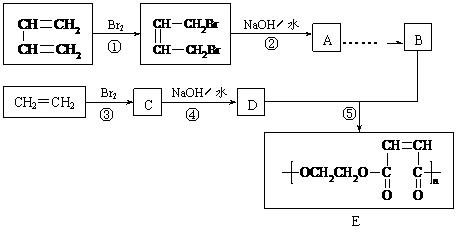
请回答:
(1)反应④的反应类型________________。
(2)A的结构简式_______________________。
(3)反应③的化学方程式
___________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com