
题目列表(包括答案和解析)
5. 目前人类已发现的非金属元素除稀有气体外 , 共有 16 种 ,下列对这16种非金属元素的相关判断:
①都是主族元素 , 最外层电子数都大于4
②单质在反应中都只能作氧化剂
③氧化物常温下都是气态 , 所以又叫都气态氢化物
④氧化物常温下都可以与水反应生成酸
A 有①②正确 B. 只有①③正确
C. 只有③④正确 D. ①②③④均不正确
4. 测定相对分子质量的常用方法之一是凝回点下降法。例如水是常用的溶剂 , 当水中溶解了某种不挥发的溶质时 ,水的凝固点 (即冰点) 即会下降 , 海水在 0℃时不会结冰就是这个原因。凝固点下降的程度与溶质的分子数有关 ,而与溶质是何种物质无关 , 这就是溶液的依数性。当溶剂的量确定时 , 凝固点的降低值与溶质分子数成正比。己知 10.0 g 樟脑中
溶解 0.412 g萘 , 凝固点下降了13 °C, 即么 , 组成为 C7H602 的有机物 0.23g 溶于 15.6 g 樟脑中 , 凝固点下降约多少 ( 己知萘相对分子质量为 : 128)
A.5 ℃ B.8℃ C.7℃ D.12℃
3. 2005 年 10 月 12 日我国成功发射了第二艘载人航夭飞船-- " 神州六号 ", 实现了双人
多天太空旅行。这标志着中国人的太空时代又前进了一大步。发射 " 神六 " 时用肼 (N2H4) 作为火箭发动机的燃料 , NO2 为氧化剂 , 反应生成 N2和水蒸气。
已知 : N2(g) + 202(g) = 2N02(g); ΔH = +67.7kJ/mol
N2H4(g) + 02(g) = N2(g) + 2H20(g); ΔH= -534kJ/mol 下列关于肼和 N02 反应的热化学方程式中 , 正确的是
A 、 2N2H4(g) + 2N02(g) = 3N2(g) + 4H20(I); ΔH = - 11 35.7kJ/mol B 、 2N2H4(g) + 2N02(g) = 3N2(g) + 4H20(g); ΔH= -1000.3kJ/mol c 、 N2H4(g) + N02(g) = 3/2N2(g) + 2H20(l); ΔH = -11 35.7kJ/mol D 、 2N2H4(g) + 2N02(g) = 3N2(g) + 4H20(g); ΔH =-1135.7kJ/mol
2. 最近广东北江发生严重的水体铺污染事件 , 专家确定用 1200 吨的聚合铁 { 简称 PFS, 化学式为 : [Fe2(OH)n(S04)3-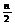 ]m' n<5,m<10} 分批加入 , 利用 PFS 在水体中形成絮状物 ,
]m' n<5,m<10} 分批加入 , 利用 PFS 在水体中形成絮状物 ,
以吸附镉离子。结合题中信息 , 下列说法不正确的是:
A. 10848Cd 核索中中子数为 60
B. 含镉废电池应进行回收处理
C. PFS 中铁显十 2 价
D. 实验室由 FeS04 溶液制 PFS 需经过氧化、水解和聚合的过程
1. 用即热饭盒盛装食物 , 可以得到热烘烘的饭菜。原因是即热饭盒的底部装入混有镁、 铁粉末的高密度聚乙烯 , 进行简单的操作后水和镁就会发生剧烈的化学反应 , 放出热量便可使食物变热 , 其中铁可能是
A. 一种反应物 B. 催化剂
c. 起导热作用 D. 增大镁与水分子的接触机会
26、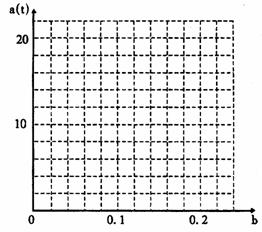 (1)3.2t 16800m3
(1)3.2t 16800m3
 (2)a=20-100b
0.067<b<0.2
(2)a=20-100b
0.067<b<0.2






 (3)
(3)
21、 (1)MnO2 +4HCl(浓) 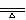 MnO2 +Cl2↑+2H2O (2)浓硫酸 (3)增大反应接触面
MnO2 +Cl2↑+2H2O (2)浓硫酸 (3)增大反应接触面
(4)水浴加热 (5)防止空气中水蒸气进入并吸收残留余的氯气。
23 (14分)(1) H O (2分)
(2)
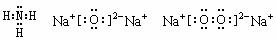 或氮化钠、氢化钠的电子式也对
或氮化钠、氢化钠的电子式也对
(3) NH4NO3 NH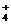 +OH―
+OH―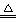 NH3↑+H2O (4)原子晶体 (以上每空2分)
NH3↑+H2O (4)原子晶体 (以上每空2分)
|
(2) 2HIO +H2O2=I2+ O2↑+ 2H2O 2H2O2=== O2↑+ 2H2O
|
2I-+2H++H2O2=I2+ 2H2O(写化学方程式不得分) 2H2O2=== O2↑+ 2H2O
20.(8分)(各2分)
(1)A、B、D、F、G、H、J;坩埚钳、泥三角、药匙
(2)偏高; A、D
19、B、C、F、
26.某化工厂以硫磺为原料生产硫酸.设空气中的氧气的体积分数为0.20,且不考虑各生产阶段的物料损失.试完成下列各题:
(1)如果该厂生产98%的硫酸10t。
①需要原料硫磺的质量是________________t。
②需要消耗空气的体积(标准状况)为________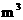 。
。
(2)如果该厂每天生产98%的硫酸at,在生产过程中为了使硫充分燃烧,且在下一步催化氧化时不再补充空气,要求硫燃烧后的混合气体中氧气的体积分数为b。已知该厂每天消耗空气2.24×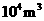 (标准状况)。
(标准状况)。
①写出a和b的关系式。
②在图中画出a和b的关系曲线。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com