
题目列表(包括答案和解析)
5.X、Y是元素周期表ⅦA族中的两种元素。下列叙述中能说明X的非金属性比Y强的是( )
A.X原子的电子层数比Y原子的电子层数多
B.X的氢化物的沸点比Y的氢化物的沸点低
C.X的气态氢化物比Y的气态氢化物稳定
D. Y的单质能将X从NaX的溶液中置换出来
4.向一种溶液中滴加另一种溶液后,溶液的颜色不发生变化的是( )
A.碳酸氢钠溶液中滴加稀盐酸 B.硫酸铁溶液中滴加硫氰化钾溶液
C.碘水中滴加淀粉碘化钾溶液 D.高锰酸钾酸性溶液中滴加亚硫酸钠溶液
3.下列各组物质中,将前者加入后者时,无论前者是否过量,都能用同一个离子方程式表示的是( )
A.稀盐酸 Na2CO3溶液 B.稀H2SO4溶液 NaAlO2溶液
C.Cu FeCl3溶液 D.浓氨水 AgNO3溶液
2. 下列叙述正确的是( )
A.在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原
B.有单质参加或生成的反应一定属于氧化还原反应
C.失电子难的原子,获得电子的能力一定强
D.元素由化合态变成游离态时,它可能被氧化,也可能被还原
1.下列各项中表达正确的是( )
A.F-的结构示意图: B.CO2的分子模型示意图:
B.CO2的分子模型示意图:
C.NaCl的电子式: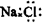 D.N2的结构式: :N≡N:
D.N2的结构式: :N≡N:
26.(6分)在25℃时,用铂电极电解密度为ρg/cm3的一定量的Na2SO4饱和溶液。一段时间后,阴极析出amol气体,同时溶液中析出bgNa2SO4·10H2O。如果在这一过程中温度不变,试求:
(1)此时Na2SO4溶液中溶质量分数为多少?
(2)此时Na2SO4溶液中物质的量浓度是多少?
(3)25℃时,Na2SO4的溶解度是多少?
25.(4分)用足量的锌粒与一定量的稀硫酸反应制取氢气,为了提高反应速率,但又不影响生成氢气的总量,在实验中可采取哪些措施(至少写出两种)?并说明理由。
24.(9分)根据实验室中测定硫酸铜晶体里结晶水含量的实验,填写下列空白。
(1)从下列仪器中选出实验所需仪器(用标号字母填空) 。
A.托盘天平(磕码) B.泥三角
C.试管夹 D.酒精灯
E.蒸发皿 F.玻璃棒
G.坩埚 H.干燥器
I.石棉网 J.三脚架。
除上述仪器外,还需要的仪器是 。
(2)某学生实验后得到以下数据:
|
加热前质量 |
加热后质量 |
|
|
W1(容器质量) |
W2(容器质量+晶体质量) |
W3(容器质量+无水CuSO4质量) |
|
5.4g |
7.9g |
6.8g |
测定结晶水的质量分数计算式(用W1、W2、W3表示)为:
w(H2O)= 。
该生实验测定结果误差是 (填“偏高”或“偏低”或“不偏”。)
(3)该学生产生实验误差的原因可能是(填写字母) 。
A.加热前称量时容器未完全干燥
B.最后两次加热后的质量相差较大(大于0.1g)
C.加热后容器未放入干燥器中冷却
D.加热过程中晶体有少量溅失
23.(4分)某氯碱厂,以石灰石,食盐和水为原料制取漂白粉。请写出有关反应的化学方程式。
22.(6分)有一包粉状的混合物,可能含有MgCl2、FeCl3、NaOH、CuSO4、Al2(SO4)3、KNO3、CaCO3、NaCl中的两种或多种。将混合物少量置于水中溶解,得无色透明溶液。再将所得溶液分为两份,一份中通入CO2,有白色沉淀出现,滴入稀盐酸,沉淀消失;另一份中加入BaCl2溶液,同样有白色沉淀出现,此沉淀不溶于稀硝酸。以此推断:
(1)原混合物中肯定有 ;
(2)原混合物中肯定没有 ;
(3)原混合物中,不能肯定是否含有 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com