
题目列表(包括答案和解析)
16、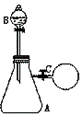 如右图所示,在抽滤瓶A中充满等体积的H2S和NO气体,分液漏斗B中盛有KI溶液,在抽滤瓶的支管处通过橡胶管连接一个盛有O2的气囊C(其最大容积约与抽滤瓶相等),夹紧。加入KI溶液后,再打开止水夹并振荡锥形瓶,下列各化学方程式肯定不符合装置内发生的化学变化事实的是
如右图所示,在抽滤瓶A中充满等体积的H2S和NO气体,分液漏斗B中盛有KI溶液,在抽滤瓶的支管处通过橡胶管连接一个盛有O2的气囊C(其最大容积约与抽滤瓶相等),夹紧。加入KI溶液后,再打开止水夹并振荡锥形瓶,下列各化学方程式肯定不符合装置内发生的化学变化事实的是
A. 2NO + O2 → 2NO2
B. H2S + HNO3 → HNO2 + S↓+ H2O
C. 2KI + 2NO2 → 2KNO2 + I2
D. 2H2S + 3O2 → 2SO2 + 2H2O
15、常温下将相同体积的氨水和盐酸混合,发现c(NH4+)=c(Cl-),下列叙述中正确的是
A.混合溶液的pH>7 B.氨水的电离度减小
C.混合溶液还能继续中和盐酸 D.氨水和盐酸中溶质的物质的量浓度相等
14、下列离子方程式正确的是
A.硫化氢通入氯化亚铁溶液中 H2S+Fe2+→FeS↓+2H+
 B.将苯酚溶液滴入碳酸钠溶液中直至过量
B.将苯酚溶液滴入碳酸钠溶液中直至过量 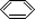 +CO32-→
+CO32-→ +HCO3-
+HCO3-
C.氯气通入冷的氢氧化钠溶液中 2Cl2+2OH-→3Cl-+ClO-+H2O
D.碳酸氢镁溶液中加入过量石灰水
Mg2++2HCO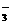 +Ca2++2OH-→CaCO3↓+2H2O+MgCO3↓
+Ca2++2OH-→CaCO3↓+2H2O+MgCO3↓
13、 恒温下,反应 aX(g) bY(g) + cZ(g) 达到平衡,把容器体积压缩到原来的1/2,达到新平衡时X的物质的量浓度从0.1 mol/L变化到0.19 mol/L,下列判断正确的是
恒温下,反应 aX(g) bY(g) + cZ(g) 达到平衡,把容器体积压缩到原来的1/2,达到新平衡时X的物质的量浓度从0.1 mol/L变化到0.19 mol/L,下列判断正确的是
A. a > b + c B. a < b + c
C. a = b + c D. a = b = c
12、为确定下列物质置于空气中是否已变质,所选检验试剂(括号内物质)不能达到目的的是
A.FeCl2溶液(KSCN) B.Na2SO3溶液(BaCl2)
C.KOH(盐酸) D.HCHO溶液(石蕊试液)
11、关于如图所示装置的叙述中正确的是
A. 若仅闭合K2接通回路,铁电极上发生氧化反应
B. 若仅闭合K2接通回路,炭极附近溶液变红
C. 若仅闭合K1接通回路,电流由炭极流向铁极
D. 若仅闭合K1接通回路,铁为阴极,炭为阳极
10、“吊白块”的主要化学成分是 NaO-CH2-SO3H ,它虽能使粉丝漂白,但会在粉丝中残留甲醛等有毒物质,严重危害人体健康。吊白块可由NaHSO3和HCHO在一定条件下通过化学反应制得: NaHSO3 + HCHO → NaO-CH2-SO3H。该反应的类型属于
 A.取代反应 B.加成反应
A.取代反应 B.加成反应
C.聚合反应 D.消去反应
9、下列工业生产的主要过程中,不需要催化剂就能顺利实现的是
A.硫铁矿制硫酸 B.乙烯的水化 C.氨碱法制纯碱 D.油脂的氢化
8、与阿伏加德罗常数值最为接近的是
A. 0.2 mol CH4中所含的原子总数
B. 标准状况下, 22.4 L SO3中所含的分子数
C. 1 L 1 mol/L CH3COOH溶液中的溶质分子数
D. 0.1mol CH3+(碳正离子)中含有的电子数
7、巳知某pH=2的溶液中存在较多的SO42-和NO3-,该溶液中还可能大量存在的离子组是
A.Al3+、CH3COO-、Cl- B.Mg2+、Ba2+、Br-
C.Mg2+、Cl-、I- D.Na+、NH4+、Cl-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com