
题目列表(包括答案和解析)
6.下列为某同学根据中学化学教材中的数据所做的判断,其中错误的是
A.根据溶解度数据,判断长时间煮沸Mg(HCO3)2溶液所得的沉淀是MgCO3还是Mg(OH)2
B.根据沸点数据,判断能否用分馏的方法分离一些液体混合物
C.根据反应热数据,判断不同反应的反应速率的大小
D.根据相对分子质量数据,判断组成和结构相似的物质的熔点和沸点的高低
5.氯酸钾跟浓盐酸反应生成氯气,化学方程式为:KClO3+6HCl=KCl+3Cl2↑+3H2O若反应使用的是K37ClO3和H35Cl,则所得氯气的摩尔质量(g·mol-1)约为:
A.70.7 B.71.0 C.72.0 D.73.3
4.要提纯下列物质(括号内物质为杂质),实验操作最合理的是
A.CO2(SO2):通入盛有品红溶液的洗气瓶
B.已烷(已烯):加入足量的溴水,充分振荡,静置分层后分离
C.硫酸铁溶液(硫酸亚铁):通入足量的氯气,充分反应后加热,使多余的氯气逸出。
D.Mg(OH)2[Ca(OH)2]:放入水中调成浆状后,加入足量MgCl2溶液,充分搅拌,过滤,沉淀用蒸馏水洗涤
3.设NA为阿伏加德罗常数,下列说法正确的是
A.常温常压下,8g氦气所含有的中子数目为4NA
B.标准状况下,11.2L臭氧中含有的氧原子数 目为3NA
C.0.1mol·L-1CH3COONa溶液中阴离子总数约为0.2N A
D.用NaOH溶液吸收氯气22.4L,反应中转移的电子数目为NA
2.若不断地升高温度,实现“雪花→水→水蒸气→氧气和氢气”的变化。在变化的各阶段被破坏的粒子间的相互作用依次是
A.氢键;分子间作用力;非极性键 B.氢键;氢键;极性键
C.氢键;极性键;分子间作用力 D.分子间作用力;氢键;非极性键
1.据报道,全球每年因发生金属腐蚀而造成的直接经济损失达数千亿美元。下列各电极反应式中,能表示铁的电化学腐蚀的是
①Fe-2e-=Fe2+ ②2H+ + 2e- = H2↑ ③ Fe + 2Fe3+ = 3Fe2+
④2H2O + O2 + 4e- = 4OH- ⑤4OH- - 4e- = 2H2O + O2↑
A.①②⑤ B.②③④ C.①②④ D.①③⑤
34.有铁和氧化铁组成的粉末状混合物19.2g,向其中加入250ml未知浓度的稀硫酸,当固体全部溶解时,放出3.36L氢气(标准状况)。经测定,加入的硫酸实际上消耗了3/5,且反应后的溶液中不含三价铁离子,求:(l)混合物中铁和氧化铁的质量各为多少?(2)所加稀硫酸的物质的量浓度是多少?
33.5.3g某烃完全燃烧后得到标准状况下8.96L的CO2气体,该烃的蒸气密度是氢气的53倍。求该烃的分子量和分子式。
32.请利用下图中的仪器及试剂组装成一套系列实验装置。其实验步骤是;先制取纯净、干燥的Cl2(不收集),再试验该氯气能否使干、湿两种有色布条褪色。试回答下列问题:
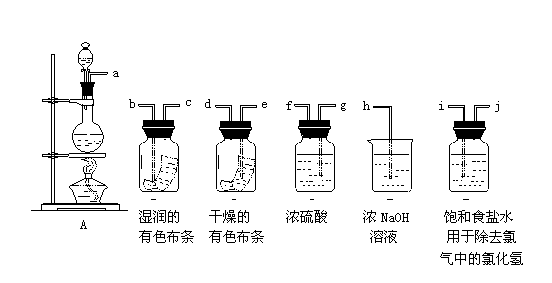
(l)按气体从左到右的流向将各装置依次连接起来(填接口标号):
a接__,__接__,__接__,__接__,__接__;
(2)分液漏斗中所盛液体是___________;
(3)烧瓶中发生反应的化学方程式是:___________________________________________.
(4)D装置的作用是________________;
E装置的作用是________________;
(5)C瓶中的现象是_________________;
B瓶中的现象是_________________;
以上实验现象说明起漂白作用的物质是(写化学式)____________。
|




|


 A
B
C
D
A
B
C
D
Ag O2
|


 E
F
E
F
试回答:
(1)A、F的结构简式为:
A、_____________,F__________________。
(2)写出下列转化的化学方程式,并指明有机反应类型:
B→C______________________________,反应类型。
C→D______________________________,反应类型。
31. 有A、B、C、D四瓶失去标签的无色溶液,它们分别是硝酸钡溶液、氨水、硫酸铝溶液和氢氧化钠溶液中的一种,其相互关系如下图所示:
|
|


 先有沉淀后消失
先有沉淀后消失
 D
D
|

 白色沉淀
沉 沉淀不溶解
白色沉淀
沉 沉淀不溶解
A是__________溶液;B是___________溶液;
C是__________溶液;D是___________溶液。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com