
题目列表(包括答案和解析)
12.下列叙述正确的是
A.直径介于1 nm-10 nm之间的微粒称为胶体
B.电泳现象可证明胶体属于电解质溶液
C.利用丁达尔效应可以区别溶液与胶体
D.胶体粒子很小,可以透过半透膜
11.下列叙述正确的是
A.NH3是极性分子,分子中N原子处在3个H原子所组成的三角形的中心
B.CCl4是非极性分子,分子中C原子处在4个Cl原子所组成的正方形的中心
C.H2O是极性分子,分子中O原子不处在2个H原子所连成的直线的中央
D.CO2是非极性分子,分子中C原子不处在2个O原子所连成的直线的中央
10.已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化
H2O2 →H2O IO3- →I2 MnO4-→Mn2+ HNO3→NO
如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是
A.H2O2 B.IO3- C.MnO4- D.HNO3
9. 某氯化镁溶液的密度为1.18 g•cm-3 ,其中镁离子的质量分数为5.1%。300 mL该溶液中Cl- 离子的物质的量约等于
A.0.37 mol B.0.63 mol C.0.74 mol D.1.5 mol
8. 下列反应的离子方程式书写正确的是
A.氯化铝溶液中加入过量氨水:Al3+
+ 4NH3•H2O
AlO2- + 4NH4+
+ 2H2O
B.澄清石灰水与少量苏打溶液混合:Ca2+ + OH- + HCO3-
CaCO3↓+ H2O
C.碳酸钙溶于醋酸:CaCO3
+ 2H+ Ca2+ + CO2↑ + H2O
D.氯化亚铁溶液中通入氯气:2Fe2+
+ Cl2 2Fe3+ + 2Cl-
7. 将纯水加热至较高温度,下列叙述正确的是
A.水的离子积变大、pH变小、呈酸性
B.水的离子积不变、pH不变、呈中性
C.水的离子积变小、pH变大、呈碱性
D.水的离子积变大、pH变小、呈中性
6.
反应 2A(g)+ B(g)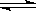 2C(g);△H>0。下列反应有利于生成C的是
2C(g);△H>0。下列反应有利于生成C的是
A.低温、低压 B.低温、高压 C.高温、高压 D.高温、低压
29.(15分)
四川有丰富的天然气资源。以天然气为原料合成尿素的主要步骤如下图所示(图中某些转化步骤及生成物未列出):
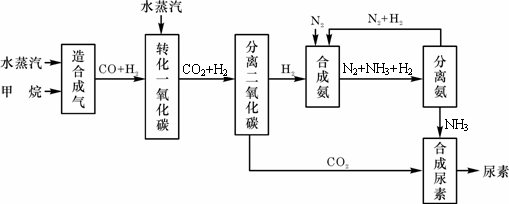
请填写下列空白:
(1)已知0.5 mol甲烷与0.5 mol水蒸汽在t ℃、p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量,该反应的热化学方程式是:
。
(2)在合成氨的实际生产过程中,常采取的措施之一是:将生成的氨从混合气体中及时分离出来,并将分离出氨后的氮气和氢气循环利用,同时补充氮气和氢气。请运用化学反应速率和化学平衡的观点说明采取该措施的理由:
。
(3)当甲烷合成氨气的转化率为75%时,以5.60×107 L甲烷为原料能够合成 L氨气。(假设体积均在标准状况下测定)
(4)已知尿素的结构简式为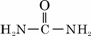 ,请写出两种含有碳氧双键的尿素的同分异构体的结构简式:
,请写出两种含有碳氧双键的尿素的同分异构体的结构简式:
① ;② 。
28.(12分)
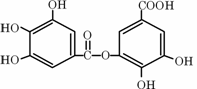 四川盛产五倍子。以五倍子为原料可制得化合物A。A的结构简式如右图所示:
四川盛产五倍子。以五倍子为原料可制得化合物A。A的结构简式如右图所示:
请解答下列各题:
(1)A的分子式是 。
(2)有机化合物B在硫酸催化条件下加热发生酯化反应可得到A。请写出B的结构简式:
(3)请写出A与过量NaOH溶液反应的化学方程式:
(4)有机化合物C是合成治疗禽流感药物的原料之一。C可以看成是B与氢气按物质的量之比1∶2发生加成反应得到的产物。C分子中无羟基与碳碳双键直接相连的结构,它能与溴水反应使溴水褪色。请写出C与溴水反应的化学方程式。
27.(15分)
A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1∶2。在一定条件下,各物质之间的相互转化关系如右(图中部分产物未列出):
请填写下列空白:
(1)A是 ,C是 。
(2)H与盐酸反应生成E的化学方程式是 。
(3)E与F反应的化学方程式是 。
(4)F与G的水溶液反应生成I和D的离子方程式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com