
题目列表(包括答案和解析)
13.1mol某烃在氧气中充分燃烧,需要消耗氧气179.2 L(标准状况下)。它在光照的条件下与氯气反应能生成三种不同的一氯取代物。该烃的结构简式是
A 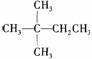 B CH3CH2CH2CH2CH3
B CH3CH2CH2CH2CH3
C 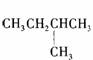 D CH3-
D CH3- -CH3
-CH3
12.在一定条件下,分别以高锰酸钾、氯酸钾、过氧化氢为原料制取氧气,当制得同温、同压下相同体积的氧气时,三个反应中转移的电子数之比为
A 1︰1︰1 B 2︰2︰1 C 2︰3︰1 D 4︰3︰2
11.在一定温度下,向a L密闭容器中加入1mol X气体和2 mol Y气体,发生如下反应:X(g)+2Y(g)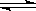 2Z(g)此反应达到平衡的标志是
2Z(g)此反应达到平衡的标志是
A 容器内压强不随时间变化
B 容器内各物质的浓度不随时间变化
C 容器内X、Y、Z的浓度之比为1︰2︰2
D 单位时间消耗0.1mol X同时生成0.2mol Z
10.在原电池和电解池的电极上所发生的反应,同属氧化反应或同属还原反应的是
A 原电池的正极和电解池的阳极所发生的反应
B 原电池的正极和电解池的阴极所发生的反应
C 原电池的负极和电解池的阳极所发生的反应
D 原电池的负极和电解池的阴极所发生的反应
9.下列离子方程式书写正确的是
A 碳酸氢钙溶液中加入过量的氢氧化钠溶液:HCO3-+OH-=CO32-+H2O
B 氯化铁溶液中通入硫化氢气体:2Fe3++S2-=2Fe2++S↓
C 次氯酸钙溶液中通人过量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO
D 氯化亚铁溶液中加入硝酸:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑
8.将40 mL 1.5 mol·L-1的CuSO4溶液与30 mL 3 mol·L-1的NaOH溶液混合,生成浅蓝色沉淀,假如溶液中[Cu2+]或[OH-]都已变得很小,可忽略,则生成沉淀的组成可表示为
A Cu(OH)2 B CuSO4·Cu(OH)2
C CuSO4·2Cu(OH)2 D CuSO4·3Cu(OH)2
7.周期表中16号元素和4号元素的原子相比较,前者的下列数据是后者的4倍的是
A 电子数 B 最外层电子数 C 电子层数 D 次外层电子数
6.室温时,0.01 mol·L-1某一元弱酸的电离度为1%,则下列说法正确的是
A 上述弱酸溶液的pH=4
B 加入等体积0.01 mol·L-1 NaOH溶液后,所得溶液的pH=7
C 加入等体积0.01 mol·L-1 NaOH溶液后,所得溶液的pH>7
D 加入等体积0.01 mol·L-1 NaOH溶液后,所得溶液的pH<7
5.R、X、Y和Z是四种元素,其常见化合价均为+2价,且X2+与单质R不反应;X2++Z=X+Z2+;Y+Z2+=Y2++Z。这四种离子被还原成0价时表现的氧化性大小符合
A R2+>X2+>Z2+>Y2+ B X2+>R2+>Y2+>Z2+
C Y2+>Z2+>R2+>X2+ D Z2+>X2+>R2+>Y2+
4.六氯苯是被联合国有关公约禁止或限制使用的有毒物质之一。下式中能表示六氯苯的是
A 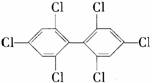 B
B 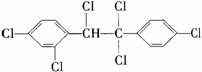
C 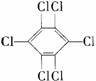 D
D 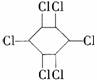
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com