
题目列表(包括答案和解析)
4..(10分)
某同学为了验证海带中含有碘,拟进行如下实验,请回答相关问题。
⑴ 第1步:灼烧。操作是将足量海带灼烧成灰烬,该过程中将使用到的硅酸盐质实验仪器有 _________________(填代号,限填3项)
A.试管 B.瓷坩埚 C.坩埚钳 D.铁三角架
E.泥三角 F.酒精灯 G.烧杯 H.量筒
⑵ 第2步:I- 溶液的获取。操作是_________________________________。
⑶ 第3步:氧化。 操作是依次加入合适的试剂,下列氧化剂最好选用_________(填代号),
A.浓硫酸 B.新制氯水 C.KMnO4溶液 D.H2O2
理由是________________________________________________。
⑷ 碘单质的检验。 操作是取少量第3步的溶液,滴加淀粉溶液,如果溶液显蓝色,则证明海带中含碘。
3.在实验室里制取某些有毒气体时,为了尽量防止毒气逸散造成空气污染,有人设计了如下图所示的装置[Ⅰ]。并设想用[Ⅱ]或[Ⅲ]两种简易装置代替[Ⅰ]的b-c部分,以求达到同样的目的。
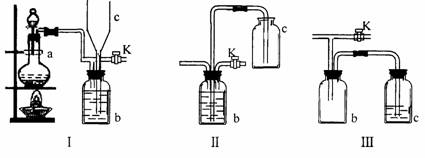
试回答:
(1)若用[Ⅰ]取氯气,b瓶加入的液体一般为 ______________。在选取试剂正确且适量的前题下,反应开始后,当关闭活塞K时如若发现c中液面不明显上升,你分析可能的原因是___________________检查的简单方法是_____________
(2)装置[Ⅰ]中b能防止多余气体逸散的原因是: _________________
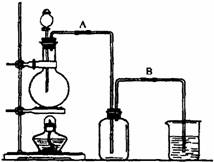
2.某校化学兴趣小组用浓盐酸与二氧化锰加热反应来制取并收集氯气,装置如下:
(1)写出该反应的化学方程式 。
(2)上述反应中,还原剂是 ,若有1mol氧化剂参加反应,转移的电子的物质的量是 mol。
(3)实验开始前,某学生对装置进行了气密性检查。方法是:连接好装置后,用弹簧夹夹住 处(填“A”或“B")橡皮管;向分液漏斗中加水并打开活塞,当加到一定量时,停止加水,静置观察,当观察到分液漏斗中 时,表明该装置不漏气。
(4)兴趣小组的某些同学准备在烧杯中加入下列溶液中的一种来吸收残余氯气,你认为其中错误的是(填序号) 。
A 氢氧化钠溶液 B 碳酸钠浓溶液 C 浓硫酸
129.(8分)某同学拟用氯化钙固体、碳酸钠溶液和稀硝酸等试剂,先制得碳酸钙,最终制得纯净的硝酸钙晶体。
(1)写出制取过程中反应的离子方程式:
、
(2)请帮助该同学完成下列实验操作步骤(不要求回答使用的仪器)
①用蒸馏水完全溶解CaCl2后,加入 。
②将反应后的混合物过滤,并用适量蒸馏水洗涤沉淀至无Cl-。
 ③加入
,使沉淀完全溶解。
③加入
,使沉淀完全溶解。
④ ,得到纯净的硝酸钙晶体。
6..(14分)A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有氧化性。下述为相关实验步骤和实验现象:
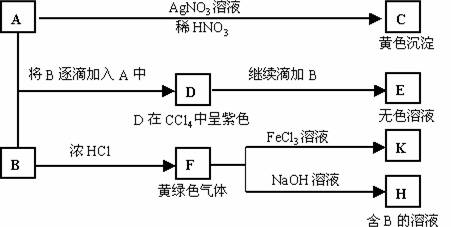
请回答:
(1)写出A、B和C的化学式:A ,B ,C 。
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:
, 。
(3)写出将SO2气体通入K溶液中发生反应的离子方程式:
(4)写出由F→H的化学方程式: 。
5.(1)1986年,化学上第一次用非电解法制得氟气,试配平该反应的化学方程式:
K2MnF6+ SbF5 - KSbF6+ MnF3+ F2
反应中 元素被还原.
(2) 氰(CN)2、硫氰(SCN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素[如(SCN)2+ H2O==HSCN+HSCNO]它们阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-.试写出:
①(CN)2与KOH溶液反应的化学方程式
②NaBr和KSCN的混合溶液中加入(CN)2,反应的离子方程式
4.已知:
①A、B、C、D四种物质均含元素X,有的还可能含有元素Y、Z。元素Y、X、Z的原子序数依次递增。
②X在A、B、C、D中都不呈现它的最高化合价。
③室温下单质A与某种常见一元强碱溶液反应,可得到B和C。
④化合物D受热催化分解,可制得元素Y的单质。
(1)元素X是 ,Z是 。
(2)写出③中反应的化学方程式: 。
(3)写出④中反应的化学方程式: 。
3..A、B、C、D、E分别代表5种微粒,每种微粒中都含有18个电子。其中A和C都是由单原子形成的阴离子,B、D和E都是分子;又知在水溶液中A跟B反应可生成C和D;E具有强氧化性。请回答:
(1)用化学符号表示上述5种微粒:
A ,B ,C ,D ,E 。
(2)在水溶液中A跟B反应的离子方程式是: 。
2.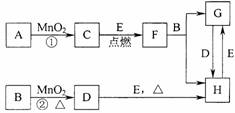 .(9分)下图所涉及的物质均为中学化学中的常见物质,其中C为O2、D为C12、E为Fe单质,其余为化合物。它们存在如下转化关系,反应中生成的水及次要产物均已略去。
.(9分)下图所涉及的物质均为中学化学中的常见物质,其中C为O2、D为C12、E为Fe单质,其余为化合物。它们存在如下转化关系,反应中生成的水及次要产物均已略去。
(1)写出有关物质的名称或化学式:
B ,F ,H 。
(2)指出MnO2在相关反应中的作用:反应①中是 剂,反应②中是 剂。
(3)若反应①是在加热条件下进行,则A是 ;若反应①是在常温条件下进行,则A是 。
(4)写出B与MnO2共热获得D的化学方程式 。
1.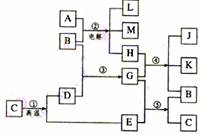 根据下列反应框图填空,已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应。
根据下列反应框图填空,已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应。
(1)单质L是 。
(2)化合物B是 。
(3)图中除反应①以外,还有两个用于工业生产的反应,是 和 (填代号)。
它们的化学反应方程式分别是 和 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com