
题目列表(包括答案和解析)
5. 在一定条件下,可逆反应A2(g)+B2(g) 2C(g)达到平衡时,各物质的浓度为:c(A2)=0.5mol/L,
c(B2)=0.1mol/L, c(C)=1.6mol/L,若用a、b、c(均大于零)分别表示A2、B2、C的初始浓度,则:
在一定条件下,可逆反应A2(g)+B2(g) 2C(g)达到平衡时,各物质的浓度为:c(A2)=0.5mol/L,
c(B2)=0.1mol/L, c(C)=1.6mol/L,若用a、b、c(均大于零)分别表示A2、B2、C的初始浓度,则:
(1)a、b、c应满足的关系式是: 。
(2)a的取值范围是 。
讨论:
4. 容积反应容器中,要求通过调节体系温度使A(g)+2B(g) 2C(g)达到平衡时保持气体总物质的量为12mol。现向反应容器中通人6.5molA、xmolB和2molC。欲使起始反应向逆反应方向移动,x的取值范围为:
。
容积反应容器中,要求通过调节体系温度使A(g)+2B(g) 2C(g)达到平衡时保持气体总物质的量为12mol。现向反应容器中通人6.5molA、xmolB和2molC。欲使起始反应向逆反应方向移动,x的取值范围为:
。
3、在一个密闭容器中充入2molSO2、1molO2和2molSO3,在一定条件下发生反应:
 2SO2+O2 2SO3,则最终生成SO3的物质的量的范围是
。
2SO2+O2 2SO3,则最终生成SO3的物质的量的范围是
。
小结:
思维方法之三:大于零原则(可逆反应中的任何物质的物质的量总大于零)
练习
3. 有两只密闭容器A和B,A容器有一个移动的活塞,使容器内保持恒压,B容器保持恒容。起始时这两只容器分别充入等量的体积比为2:1的SO2和O2混合气体,并使A和B容积相等,在保持400oC的条件下使之发生如下反应:2SO2+O2 2SO3;填写下列空白:
有两只密闭容器A和B,A容器有一个移动的活塞,使容器内保持恒压,B容器保持恒容。起始时这两只容器分别充入等量的体积比为2:1的SO2和O2混合气体,并使A和B容积相等,在保持400oC的条件下使之发生如下反应:2SO2+O2 2SO3;填写下列空白:
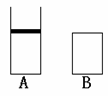 (1)达到平衡时所需时间,A容器比B容器 ,A容器中SO2转化率比B容器 。
(1)达到平衡时所需时间,A容器比B容器 ,A容器中SO2转化率比B容器 。
(2)达到(1)所述平衡后,若向容器中通人数量不多的氩气,A容器化学平衡向 移动。B容器化学平衡: 。
(3)达到(1)所述平衡后,若向容器中充入等量的原反应气体,A中SO3百分含量 (增大、不变、减小),B中SO3百分含量 (增大、不变、减小)。
讨论:
2.在一个一定容积的密闭容器中在某温度下发生如下反应:
 CO(g)+H2O(g) CO2(g)+H2(g)
CO(g)+H2O(g) CO2(g)+H2(g)
开始时充入容器中的起始物质是
①0.1molCO,0.1molH2O ;②0.1molCO,0.2molH2O;③0.1molCO,0.1molH2O,0.1molCO2;④0.1molCO,0.5molH2O,0.1molH2; ⑤ 0.1molCO,0.1molHCO,0.1molH2 ,0.1molCO2
达到平衡时容器中H2的浓度小到大排列是: 。
结论:
思维方法之二:“先同后变”或称过渡态。进行判断时可设相同的参照标准,再根据题设条件观察变化趋势。
练习
2、 A、B、C、D四种物质皆易溶于水。在稀溶液中建立了下列化学平衡:
 A+2B+H2O
C+D
A+2B+H2O
C+D
加水稀释时平衡向 反应方向移动,其理由是:
讨论
1、可逆反应:
 2HI(g) H2(g)+I2(g)达到平衡状态,下列哪些操作不能使平衡发生移动(
)
2HI(g) H2(g)+I2(g)达到平衡状态,下列哪些操作不能使平衡发生移动(
)
(A)压强不变,充入少量H2
(B)容器体积不变,充入少量N2
(C)改变容器体积
(D)向平衡体系中充入少量NH3(g)
2..(8分)较低温度下,氯气通入石灰乳中可制得漂白粉,该反应为放热反应。某校甲、乙两化学研究性学习小组均用200 mL 12 mol/L盐酸与17.4 g MnO2在加热条件下反应制备氯气,并将制备的氯气与过量的石灰乳反应制取漂白粉,用稀NaOH溶液吸收残余的氯气.分析实验结果发现:①甲、乙两组制得的漂白粉中Ca(ClO)2的质量明显小于理论值,②甲组在较高温度下将氯气与过量的石灰乳反应,所制得的产品中Ca(ClO3)2的含量较高。
试回答下列问题:
(1)上述实验中理论上最多可制得Ca(ClO)2多少克?
(2)实验中所得到的Ca(ClO)2的质量明显小于理论值,试简要分析其可能原因,并写出可能涉及到的化学方程式。
1.将 氯化钠、溴化钾和氯化钙的混合物溶于水中,通入氯气充分反应,然后把溶液蒸干并灼烧(高温加热),灼热后残留物的质量为
氯化钠、溴化钾和氯化钙的混合物溶于水中,通入氯气充分反应,然后把溶液蒸干并灼烧(高温加热),灼热后残留物的质量为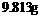 。若将此残留物再溶于水并加入足量的碳酸钠溶液,所得的沉淀经干燥后质量为
。若将此残留物再溶于水并加入足量的碳酸钠溶液,所得的沉淀经干燥后质量为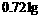 。求原混合物中各化合物质量。
。求原混合物中各化合物质量。
5..(14分)
在玻璃圆筒中盛有两种无色的互不相溶的中性液体。上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅棒,可以上下搅动液体,装置如右图。接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成。停止通电,取出电极,用搅棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。根据上述实验回答:
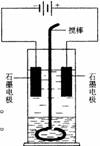 (1)阳极上的电极反应式为________________。
(1)阳极上的电极反应式为________________。
(2)阴极上的电极反应式为__________________。
(3)原上层液体是_______________________。
(4)原下层液体是______________________。
(5)搅拌后两层液体颜色发生变化的原因是______________________。
(6)要检验上层液体中含有的金属离子,其方法是_____________________,现象是________________________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com