
题目列表(包括答案和解析)
3、下列说法正确的是(NA表示阿伏加德罗常数的值) A.28g氮气所含有的原子数目为NA B.4g金属钙变成钙离子时失去的电子数目为O.1NA C.lmol甲烷的质量与NA个甲烷分子的质量之和相等
D. 标准状况下,22.4L甲烷和乙炔混合物所含的分子数为NA 4、设NA为阿佛加德罗常数,下列说法不正确的是
A 标准状况下的22.4L辛烷完全燃烧,生成二氧化碳分子数为8NA
B 18g水中含有的电子数为10NA
C 46g 二氧化氮和46g四氧化二氮含有的原子数均为3NA
D 在1L2mol/L的硝酸镁溶液中含有的硝酸根离子数为4NA
2、依照阿佛加德罗定律,下列叙述正确的是 A、同温同压下两种气体的体积之比等于摩尔质量之比 B、同温同压下两种气体的物质的量之比等于密度之比 C、同温同压下两种气体的摩尔质量之比等于密度之比 D、同温同体积下两种气体的物质的量之比等于压强之比
1、设阿佛加德罗常数的符号为NA,标准状况下某种O2和N2的混合气体m克含有b个分子,则n克该混合气体在相同状况下所占的(L)体积应是
A 22.4nb/mNA B 22.4mb/bNA C 22.4nNA/mb D nbNA/22.4m
33、下列说法正确的是
A 非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价
B 只有非金属能形成含氧酸或含氧酸盐
C 除稀有气体外的非金属元素都能生成不同价态的含氧酸
D 非金属的最高价含氧酸都具有强氧化性
阿佛加德罗常数类
32、短周期的三种元素分别为X、Y和Z,已知X元素的原子最外层只有一个电子,Y元素原子的M电子层上的电子数是它的K层和L层电子总数的一半,Z元素原子的L电子层上的电子数比Y元素原子的L电子层上电子数少2个,则这三种元素所组成的化合物的分子式不可能是
A X2YZ4 B XYZ3 C X3YZ4 D X4Y2Z7
31、X元素的阳离子和Y元素的阴离子具有相同的核外电子结构,下列叙述正确的是
A 原子序数X<Y B 原子半径X<Y C 离子半径X>Y D 原子最外层电子数X<Y
30、根据中学化学教材所附元素周期表判断,下列叙述不正确的是
A.K层电子为奇数的所有元素所在族的序数与该元素原子的K层电子数相等
B.L层电子为奇数的所有元素所在族的序数与该元素原子的L层电子数相等
C.L层电子为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相等
D.M层电子为奇数的所有主族元素所在族的序数与该元素原子的M层电子数相等
29、.在两个容积相同的容器中,一个盛有HCl气体,另一个盛有H2和Cl2的混合气体。在同
温同压下,两容器内的气体一定具有相同的
A.原子数 B.密度 C.质量 D.质子数
28、人类探测月球发现,在月球的土壤中含有较丰富的质量数为3的氦,它可以作为未来核聚变的重要原料之一。氦的该种同位素应表示为
A.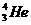 B.
B.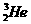 C.
C.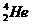 D.
D.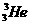
27、沼气是一种能源,它的主要成分是CH4。0.5molCH4完全燃烧生成CO2和H2O时,放出445kJ热量,则下列热化学方程式中正确的是
A 2CH4(g)+4O2(g)=2CO2(g)+4H2O(l) ΔH=+890kJ·mol-1
B CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=+890kJ·mol-1
C CH4(g)+4O2(g)=CO2(g)+2H2O(l) ΔH=-890kJ·mol-1
D 1/2CH4(g)+O2(g)=1/2CO2(g)+H2O(l) ΔH=-890kJ·mol-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com