
题目列表(包括答案和解析)
15、反应速率V和反应物浓度的关系是用实验的方法测定的,化学反应:H2+Cl2=2HCl的反应速率V可以表示为:v=k(C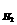 )m (C
)m (C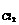 )n,式中的k为常数,m和n的值以可用下列表中数据确定之。
)n,式中的k为常数,m和n的值以可用下列表中数据确定之。
C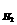 (mol/L) (mol/L) |
C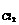 (mol/L) (mol/L) |
V(mol/L·S) |
|
1.0 |
1.0 |
1.0k |
|
2.0 |
1.0 |
2.0k |
|
2.0 |
4.0 |
4.0k |
由此可以推得,m和n的值正确的是
A、m=1
,n=2
B、m= 、n=
、n=
C、m= ,
n=1
D、m=1 ,n=
,
n=1
D、m=1 ,n=
14、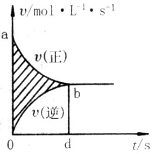 在容积为4
L的刚性密闭容器中.进行可逆反应:
在容积为4
L的刚性密闭容器中.进行可逆反应:
X (g) + 2Y(g) 2Z(g)并达到平衡在此过程中以
2Z(g)并达到平衡在此过程中以
Y的浓度改变表示的反应速率v(正)、v(逆)与时间t的关
系如图示,则图中阴影部分的面积表示
A、X的浓度的变化 B、Y的浓度的变化
C、Z的浓度的变化 D、Y的物质的量的减少
13、用某种仪器量一液体体积时,平视读数为V1mL,仰视读数为V2mL,俯视读数为V3mL,若V3>V1>V2,则所使用仪器可能是
A、容量瓶 B、量筒
C、碱式滴定管 D、以上仪器均可
12、将10 mL0.1 mol·L-1氨水与10 mL0.2 mol·L-1盐酸混合后,溶液中各种离子的物质的量浓度由大到小的顺序是
A、c(Cl-)>c(H+)>c(NH4+)>c(OH-) B、c(Cl-)>c(NH4+)>c(H+)>c(OH-)
C、c(NH4+)>C(Cl-)>c(OH-)>c(H+) D、c(H+)>c(Cl-)>c(NH4+)>c(OH-)
11、将两份质量相等的铝粉,分别加入足量的氢氧化钠和足量的稀硫酸溶液中,则它们放出的气体(相同条件下)的体积比为 ( )
A.1∶1 B.1∶2
C.1∶3 D.2∶3
10、在CH3COOH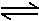 H++CH3OO-的电离平衡中,要使电离平衡右移且可采取的措施是
H++CH3OO-的电离平衡中,要使电离平衡右移且可采取的措施是
A、加入NaOH B、加入盐酸
C、加入NaAc D、加热
9、物质的量浓度相同的强酸和强碱以等体积相互反应后的溶液
A.一定呈中性 B.一定呈酸性
C.一定呈碱性 D.酸碱性无法判断
8、锌锰干电池在放电时,电池总反应方程式可以表示为:Zn+2MnO2+2NH4+ =
Zn2++Mn2O3+2NH3+H2O 在此电池放电时,正极(碳棒)上发生反应的物质是
A.Zn B.碳棒
C.MnO2和NH4+ D.Zn2+和NH4+
7、把Ba(OH)2溶液滴入明矾溶液中,使SO42-全部转化成BaSO4沉淀,此时铝元素的主要存在形式是
A Al3+ B Al(OH)3
C AlO2- D Al3+和Al(OH)3
6、25℃时,pH=2的HCl溶液中,由水电离出的H+浓度是 ( ).
A.1×10-7mol·L-1 B.1×10-12mol·L-1.
C.1×10-2mol·L-1 D.1×10-14mol·L-1.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com